Procent efter masse vand i Epsom -salt MgsO47H2O?
1. Find den molære masse af hver komponent:
* mgso₄:
* Mg:24,31 g/mol
* S:32,06 g/mol
* O:16,00 g/mol (x 4) =64,00 g/mol
* Samlet molmasse af Mgso₄ =24,31 + 32,06 + 64,00 =120,37 g/mol
* 7h₂o:
* H:1,01 g/mol (x 2 x 7) =14,14 g/mol
* O:16,00 g/mol (x 7) =112,00 g/mol
* Samlet molmasse på 7H₂O =14,14 + 112,00 =126,14 g/mol
2. Find den samlede molære masse af Epsom -salt:
* Samlet molmasse af Mgso₄ · 7H₂O =120,37 g/mol + 126,14 g/mol =246,51 g/mol
3. Beregn procentdelen efter vandmasse:
* (Mass af vand / total masse af Epsom -salt) x 100%
* (126,14 g/mol/246,51 g/mol) x 100% = 51,17%
Derfor er procentdelen af vandmasse i Epsom -salt (MGSO₄ · 7H₂O) ca. 51,17%.
 Varme artikler
Varme artikler
-
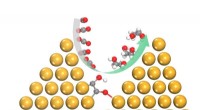 Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata -
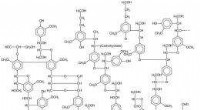 Spinding af planteaffald til kulfiber til biler, flyLignin. Billede:Wikipedia Brug af planter og træer til at fremstille produkter som papir eller ethanol efterlader en rest kaldet lignin, en komponent af plantecellevægge. Den rest af lignin er ikk
Spinding af planteaffald til kulfiber til biler, flyLignin. Billede:Wikipedia Brug af planter og træer til at fremstille produkter som papir eller ethanol efterlader en rest kaldet lignin, en komponent af plantecellevægge. Den rest af lignin er ikk -
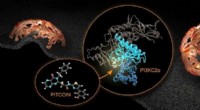 Inhibitor af lipidkinase PI3KC2a identificeret som potentiel ny behandling af tromboseKredit:Barth van Rossum Lipidkinasen PI3KC2a er et potentielt farmakologisk mål til behandling af trombose og muligvis cancer. Forskere fra Leibniz-Forschungsinstitut für Molekulare Pharmakologie (
Inhibitor af lipidkinase PI3KC2a identificeret som potentiel ny behandling af tromboseKredit:Barth van Rossum Lipidkinasen PI3KC2a er et potentielt farmakologisk mål til behandling af trombose og muligvis cancer. Forskere fra Leibniz-Forschungsinstitut für Molekulare Pharmakologie ( -
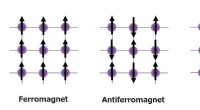 Forskere syntetiserer halvmetal uden magnetiseringSpinarrangement af magnetiske momenter i ferromagnetiske, antiferromagnetiske og ferrimagnetiske materialer. Kredit:Rie Umetsu En forskergruppe har med succes syntetiseret et halvmetal materiale og
Forskere syntetiserer halvmetal uden magnetiseringSpinarrangement af magnetiske momenter i ferromagnetiske, antiferromagnetiske og ferrimagnetiske materialer. Kredit:Rie Umetsu En forskergruppe har med succes syntetiseret et halvmetal materiale og
- Marine sensor får styr på salt
- Når vand fordampes, varmer det energi og den omgivende luft?
- NASAs nye Dellingr -rumfartøj baselineret til vejsøgning af CubeSat til Van Allen -seler
- Hvor mødes de kvindelige og mandlige sexceller?
- Revner i perovskitfilm til solceller kan let heles, undersøgelse finder
- Værts-, ledelses- eller mikrobielle egenskaber:Hvilket er dominerende i plantemikrobiomsamling?


