Hvorfor er mangan meget reaktiv?
* Elektronkonfiguration: Mangan har en kompleks elektronkonfiguration med delvist fyldte D-orbitaler. Dette gør det mindre sandsynligt, at det let mister elektroner og danner ioner sammenlignet med elementer med enklere konfigurationer.
* overfladeoxidlag: Mangan danner et beskyttende oxidlag på dets overflade, der fungerer som en barriere for yderligere reaktion. Denne passiveringseffekt hjælper med at beskytte metallet mod korrosion og yderligere reaktioner.
* relativt høje ioniseringsenergier: Ioniseringsenergierne af mangan er relativt høje, hvilket betyder, at det tager mere energi at fjerne elektroner fra dens atomer. Dette gør det mindre sandsynligt, at det deltager i reaktioner, hvor elektronoverførsel er involveret.
manganens reaktivitet påvirkes af faktorer som:
* Temperatur: Mangan bliver mere reaktiv ved højere temperaturer.
* surhed: Mangan reagerer lettere i sure miljøer.
* tilstedeværelse af oxidationsmidler: Oxideringsmidler som ilt og halogener kan fremme mangans reaktivitet.
Mens mangan ikke betragtes som meget reaktiv, spiller det stadig en betydelig rolle i forskellige industrielle processer:
* stålproduktion: Mangan bruges i stålproduktion til at forbedre dens styrke og hårdhed.
* Batterier: Mangandioxid er en nøglekomponent i tørcellebatterier.
* pigmenter: Manganforbindelser bruges som pigmenter i maling og keramik.
Selvom mangan ikke er ekstremt reaktiv som alkalimetaller, er det stadig et vigtigt og alsidigt element med forskellige anvendelser.
 Varme artikler
Varme artikler
-
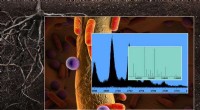 Optrævling af den molekylære kompleksitet af cellulære maskiner og miljøprocesser21-Tesla Fourier transformation ion cyclotron resonans massespektrometer (data vist til højre) vil drive den fremtidige retning af miljø, biologiske, atmosfærisk, og energiforskning. Kredit:Pacific No
Optrævling af den molekylære kompleksitet af cellulære maskiner og miljøprocesser21-Tesla Fourier transformation ion cyclotron resonans massespektrometer (data vist til højre) vil drive den fremtidige retning af miljø, biologiske, atmosfærisk, og energiforskning. Kredit:Pacific No -
 Binde molekyler lige så let som snørebåndEksempler på molekylære noder undersøgt. Kredit:UNIGE Selvom knuder kan være til gene, de er også meget nyttige, når det kommer til at binde dine snørebånd, eller når du skal sejle. I matematik, d
Binde molekyler lige så let som snørebåndEksempler på molekylære noder undersøgt. Kredit:UNIGE Selvom knuder kan være til gene, de er også meget nyttige, når det kommer til at binde dine snørebånd, eller når du skal sejle. I matematik, d -
 Nobelvindende teknik som Google Earth til molekylerRichard Henderson, en af 2017 nobelprisvindere i kemi, afholder en bakterie-rhodopsin-model forud for en pressekonference på Laboratory of Molecular Biology i Cambridge, England, Onsdag, 4. okt. 201
Nobelvindende teknik som Google Earth til molekylerRichard Henderson, en af 2017 nobelprisvindere i kemi, afholder en bakterie-rhodopsin-model forud for en pressekonference på Laboratory of Molecular Biology i Cambridge, England, Onsdag, 4. okt. 201 -
 Ny enhed identificerer bloddonorer af høj kvalitetKredit:CC0 Public Domain Blodbanker har længe kendt til donorer af høj kvalitet - individer, hvis røde blodlegemer forbliver levedygtige i længere tid i opbevaring og i modtagerens krop. Nu viser
Ny enhed identificerer bloddonorer af høj kvalitetKredit:CC0 Public Domain Blodbanker har længe kendt til donorer af høj kvalitet - individer, hvis røde blodlegemer forbliver levedygtige i længere tid i opbevaring og i modtagerens krop. Nu viser
- OO Dra er en Algol-type binær dannet gennem en ekstremt heliumfattig massetilvækst
- Frequency of Delta Waves i Sleep Study
- Earth:The Lone Pale Blue Dot?
- Videnskabelig forskning i katastrofer repræsenterer kun 0,22 procent af den globale videnskabelige …
- Hvad er jordbygning?
- Hvad er den hypotese, som forskere bruger til at forklare bevægelse af tektoniske plader?


