Brug venligst forbindelserne til at svare på, hvilket aluminiumnitrat plus calciumphosphat er lig med?
1. Identificer reaktionstypen:
Dette er en dobbeltfortrængningsreaktion . I denne type reaktion skifter de positive og negative ioner af to reaktanter.
2. Skriv den ubalancerede kemiske ligning:
AL (no₃) ₃ (aq) + Ca₃ (po₄) ₂ (aq) →?
3. Forudsig produkterne:
* Aluminium (al³⁺) -ioner fra aluminiumnitrat kombineres med phosphat (PO₄³⁻) -ioner fra calciumphosphat til dannelse af aluminiumphosphat (alpo₄) .
* Calcium (Ca²⁺) ioner fra calciumphosphat kombineres med nitratet (NO₃⁻) -ioner fra aluminiumnitrat til dannelse af calciumnitrat (CA (NO₃) ₂) .
4. Skriv den afbalancerede kemiske ligning:
2 Al (No₃) ₃ (aq) + 3 Ca₃ (Po₄) ₂ (aq) → 2 alpo₄ (s) + 3 Ca (no₃) ₂ (aq)
Forklaring af afbalancering:
* Vi har brug for 2 alpo₄ -molekyler for at afbalancere aluminium (AL) atomer.
* Vi har brug for 3 CA (NO₃) ₂ Molekyler for at afbalancere calcium (CA) atomer.
* Vi har brug for 6 ingen ioner på hver side, som allerede er afbalanceret.
* Vi har brug for 2 po₄³⁻ ioner på hver side, som allerede er afbalanceret.
5. Angiv produkterne:
Reaktionen af aluminiumnitrat og calciumphosphat producerer:
* aluminiumphosphat (alpo₄): Dette er et solidt bundfald (angivet med (er))
* calciumnitrat (CA (no₃) ₂): Dette forbliver opløst i opløsning (angivet med (aq))
Kortfattet:
Reaktionen mellem aluminiumnitrat og calciumphosphat resulterer i dannelsen af et fast bundfald af aluminiumphosphat og en opløsning af calciumnitrat.
Sidste artikelHvad er tætheden af neongas ved STP?
Næste artikelEn kemisk reaktion, der nedbryder molekyler?
 Varme artikler
Varme artikler
-
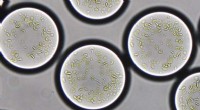 Forskere udvikler en kunstig kloroplastPlantethylacoider er indkapslet i mikrodråber på cirka 90 mikrometer i diameter. Udstyret med et sæt enzymer, de semisyntetiske kloroplaster fikserer kuldioxid ved hjælp af solenergi, efter naturens e
Forskere udvikler en kunstig kloroplastPlantethylacoider er indkapslet i mikrodråber på cirka 90 mikrometer i diameter. Udstyret med et sæt enzymer, de semisyntetiske kloroplaster fikserer kuldioxid ved hjælp af solenergi, efter naturens e -
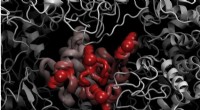 Elastisk inkohærent neutronspredning ved ILL udfordrer Lindemann-kriteriet i proteinerEt billede af lysozymproteinet, mens det smelter Proteiner er de nanomaskiner, som naturen bruger til at udføre de fleste af de processer, der er kritiske for metabolismen i celler. Et af hovedmål
Elastisk inkohærent neutronspredning ved ILL udfordrer Lindemann-kriteriet i proteinerEt billede af lysozymproteinet, mens det smelter Proteiner er de nanomaskiner, som naturen bruger til at udføre de fleste af de processer, der er kritiske for metabolismen i celler. Et af hovedmål -
 Havmuslinger er en model til forbedring af styrke, strækbarhed og vedhæftning i hydrogeler til så…Kredit:Pixabay/CC0 Public Domain Hydrogeler er overalt. De er vandelskende polymerer, der kan absorbere og tilbageholde vand, og kan findes i sådanne dagligdags forbrugerprodukter som bløde kontak
Havmuslinger er en model til forbedring af styrke, strækbarhed og vedhæftning i hydrogeler til så…Kredit:Pixabay/CC0 Public Domain Hydrogeler er overalt. De er vandelskende polymerer, der kan absorbere og tilbageholde vand, og kan findes i sådanne dagligdags forbrugerprodukter som bløde kontak -
 En termisk isoleringskomposit af hule silicapartikler blandet med cellulosefibreORNL-forskere lavede en termisk isoleringskomposit af hule silicapartikler ved at blande partiklerne med cellulosefibre. Kompositten viste sig at være meget fugtstabil og udviser potentiale for anvend
En termisk isoleringskomposit af hule silicapartikler blandet med cellulosefibreORNL-forskere lavede en termisk isoleringskomposit af hule silicapartikler ved at blande partiklerne med cellulosefibre. Kompositten viste sig at være meget fugtstabil og udviser potentiale for anvend
- Hvorfor modtager højere breddegrader mindre solstråling end lavere breddegrader?
- Internet fiberoptik kunne give værdifuld indsigt i geologiske fænomener
- Forskere undersøger den politiske kløft bag troen på klimaændringer
- Hvad er pyrokinese?
- Hvad er dataorganisation til løsning af et biologisk problem?
- Løst:Mysteriet om universets udvidelse


