Hvilke reaktanter er nødvendigt for en forbrændingsreaktion?
1. brændstof: Dette er det stof, der brænder, hvilket giver den energi, der er frigivet i reaktionen. Almindelige brændstoffer inkluderer:
* Kulbrinter (som metan, propan, benzin)
* Træ
* Ethanol
* Kul
* Naturgas
2. oxidisator: Dette er et stof, der giver det ilt, der er nødvendigt for at reaktionen kan forekomme. Den mest almindelige oxidation er iltgas (O2) .
Her er en grundlæggende kemisk ligning til forbrænding:
Brændstof + O2 → Produkter (normalt CO2 + H2O + energi)
Vigtig note: Mens ilt er den mest almindelige oxidationsmiddel, kan andre stoffer fungere som oxidationsmidler i visse situationer, såsom:
* klorgas (CL2): Kan reagere med brændstoffer som magnesium for at producere varme og lys.
* fluordas (F2): Endnu mere reaktiv end klor kan det understøtte forbrænding med en lang række stoffer.
Fortæl mig, hvis du gerne vil udforske specifikke eksempler på forbrændingsreaktioner!
Sidste artikelHvilken effekt har flydende nitrogen på molekylær kinetisk energi?
Næste artikelHvad er kogepunktet for en løsning?
 Varme artikler
Varme artikler
-
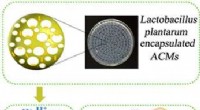 Beskyttelse af probiotika fra mavenKredit:American Chemical Society Tyndtarmen er et arnested for mikrobiel aktivitet og et mål for probiotiske behandlinger mod diarré, inflammatorisk tarmsygdom og irritabel tyktarm, blandt andre f
Beskyttelse af probiotika fra mavenKredit:American Chemical Society Tyndtarmen er et arnested for mikrobiel aktivitet og et mål for probiotiske behandlinger mod diarré, inflammatorisk tarmsygdom og irritabel tyktarm, blandt andre f -
 Test af strålingsresistens uden brug af en atomreaktorKredit:CC0 Public Domain University of Huddersfields kombinerede elektronmikroskop og ionstråleaccelerator er en facilitet i verdensklasse, der er ansvarlig for et stort og voksende globalt netvær
Test af strålingsresistens uden brug af en atomreaktorKredit:CC0 Public Domain University of Huddersfields kombinerede elektronmikroskop og ionstråleaccelerator er en facilitet i verdensklasse, der er ansvarlig for et stort og voksende globalt netvær -
 Særligt blåt lys – forsker finder ud af, at nye kemiske klynger udsender meget effektivt lysKredit:Wiley Et forskningshold fra Florida State University har opdaget, at en unik organisk-uorganisk forbindelse, der indeholder nul-dimensionelle molekylære klynger, udsender et meget effektivt
Særligt blåt lys – forsker finder ud af, at nye kemiske klynger udsender meget effektivt lysKredit:Wiley Et forskningshold fra Florida State University har opdaget, at en unik organisk-uorganisk forbindelse, der indeholder nul-dimensionelle molekylære klynger, udsender et meget effektivt -
 Bifile overflader reducerer afrimningstider i varmevekslereTime-lapse billeder af dynamisk afrimning på superhydrofobe og bifile overflader. Tidspunktet t =0 repræsenterer det tidspunkt, hvor smeltning af frost først blev observeret visuelt. Kredit:Nenad Milj
Bifile overflader reducerer afrimningstider i varmevekslereTime-lapse billeder af dynamisk afrimning på superhydrofobe og bifile overflader. Tidspunktet t =0 repræsenterer det tidspunkt, hvor smeltning af frost først blev observeret visuelt. Kredit:Nenad Milj


