Hvad er de fysiske ændringer i kalium?
Her er hvorfor:
* kalium er et element: Elementer er den enkleste form for stof og kan ikke opdeles i enklere stoffer på fysiske midler.
* Fysiske ændringer: Fysiske ændringer ændrer udseendet eller formen af et stof, men ændrer ikke dets kemiske sammensætning. Eksempler inkluderer smeltning, frysning, kogning, sublimering og kondens.
* Kemiske ændringer: Kemiske ændringer resulterer i dannelse af nye stoffer med forskellige kemiske egenskaber. Eksempler inkluderer forbrænding, rustning og madlavning.
Du kan dog tale om kaliums fysiske egenskaber:
* Matterilat: Ved stuetemperatur er kalium et blødt, sølvhvid fast fast stof.
* densitet: Kalium er et meget let metal med en densitet på 0,862 g/cm³.
* smeltepunkt: Kalium smelter ved 63,5 ° C (146,3 ° F).
* kogepunkt: Kalium koger ved 759 ° C (1398 ° F).
* reaktivitet: Kalium er meget reaktiv og reagerer med luft og vand for at danne kaliumhydroxid (KOH).
Kortfattet:
Kalium i sig selv gennemgår ikke fysiske ændringer som frysning eller kogning. I stedet har det specifikke fysiske egenskaber, der beskriver dens udseende, densitet og opførsel.
Sidste artikelHvor mange atomer er der i en sten?
Næste artikelHvordan er gæring og mælkesyreproduktion ens?
 Varme artikler
Varme artikler
-
 Gennem skueglasset:Optrævler, hvordan ioner bevæger sig i fosfatglasUndersøgelse af den mikroskopiske diffusionsmekanisme af protoner og natriumioner i fosfatglas via første principper molekylær dynamiksimulering indikerer nøglerollen af morfologien af fosfatnetvæ
Gennem skueglasset:Optrævler, hvordan ioner bevæger sig i fosfatglasUndersøgelse af den mikroskopiske diffusionsmekanisme af protoner og natriumioner i fosfatglas via første principper molekylær dynamiksimulering indikerer nøglerollen af morfologien af fosfatnetvæ -
 Udvikling af enzymer til at hjælpe med at løse planetens plastikproblemKredit:Unsplash/CC0 Public Domain Forskere fra Manchester Institute of Biotechnology (MIB) har udviklet en ny enzymteknologisk platform til at forbedre plastnedbrydende enzymer gennem rettet evolut
Udvikling af enzymer til at hjælpe med at løse planetens plastikproblemKredit:Unsplash/CC0 Public Domain Forskere fra Manchester Institute of Biotechnology (MIB) har udviklet en ny enzymteknologisk platform til at forbedre plastnedbrydende enzymer gennem rettet evolut -
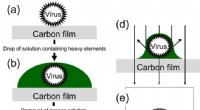 Nyt ikke-radioaktivt, neutralt reagens afslører vira i klare detaljerNegativ farvningsmetode. (a) Virioner er bundet til kulstofstøttefilmen. (b) En opløsning indeholdende tungmetaller (negativt farvningsreagens) dryppes på filmen. (c) Overskydende opløsning fjernes, o
Nyt ikke-radioaktivt, neutralt reagens afslører vira i klare detaljerNegativ farvningsmetode. (a) Virioner er bundet til kulstofstøttefilmen. (b) En opløsning indeholdende tungmetaller (negativt farvningsreagens) dryppes på filmen. (c) Overskydende opløsning fjernes, o -
 At lave tøj af mælkKredit:Piotr Łohunko I EU, beboere spilder anslået 88 millioner tons mad hvert år, ifølge de seneste skøn. Det er omkring 170 kg pr. person. Men hvad nu hvis videnskabsmænd kunne omdanne noget af
At lave tøj af mælkKredit:Piotr Łohunko I EU, beboere spilder anslået 88 millioner tons mad hvert år, ifølge de seneste skøn. Det er omkring 170 kg pr. person. Men hvad nu hvis videnskabsmænd kunne omdanne noget af
- Løsning af solenergipuslespil kan hjælpe med at redde Jorden fra strømafbrydelser på hele planet…
- Spinatprotein og brombærfarve giver juice til biohybride solceller
- Ny formørkende kataklysmisk variabel opdaget
- Hvilke planeter kan ses med det menneskelige øje?
- Hvad er forskellen mellem klipper og fossiler?
- Hvilken Nuclear Decay Emission består kun af energi?


