Hvor mange atomer er der i en sten?
* typen af sten: Forskellige mineraler har forskellige densiteter og atomkompositioner.
* Størrelsen og vægten af stenen: En lille sten vil have langt færre atomer end en stor sten.
Her er et forenklet eksempel:
Lad os sige, at vi har en lille, glat sten, der vejer 1 gram og er for det meste lavet af kvarts (siliciumdioxid, SiO2).
1. Find den molære masse: Den molære masse af SiO2 er ca. 60,08 g/mol (28,09 g/mol for Si + 2 x 16,00 g/mol for O).
2. Beregn antallet af mol: 1 g / 60,08 g / mol =0,0166 mol.
3. Brug Avogadro's nummer: En mol af ethvert stof indeholder 6,022 x 10^23 partikler (atomer, molekyler osv.). Så vores 1-gram sten har ca. 0,0166 mol x 6,022 x 10^23 atomer/mol = 1,00 x 10^22 atomer .
Dette er bare et skøn! Det faktiske antal atomer i stenen kan være højere eller lavere afhængigt af dets sammensætning og urenheder.
Sidste artikelHvad består et stof af?
Næste artikelHvad er de fysiske ændringer i kalium?
 Varme artikler
Varme artikler
-
 Undersøgelse af oxidative veje i atombrændstofDet radiokemiske behandlingslaboratorium på PNNL er hjemsted for et JEOL GrandARM-300F scanningstransmissionselektronmikroskop, her drives af materialeforsker Steven Spurgeon. Denne specialiserede fac
Undersøgelse af oxidative veje i atombrændstofDet radiokemiske behandlingslaboratorium på PNNL er hjemsted for et JEOL GrandARM-300F scanningstransmissionselektronmikroskop, her drives af materialeforsker Steven Spurgeon. Denne specialiserede fac -
 Forskere udvikler 3D-trykte biomaterialer, der nedbrydes efter behovBrune forskere har fundet en måde at 3D-udskrive indviklede midlertidige mikrostrukturer, der kan nedbrydes efter behov ved hjælp af en biokompatibel kemisk trigger. Teknikken kunne være nyttig kunne
Forskere udvikler 3D-trykte biomaterialer, der nedbrydes efter behovBrune forskere har fundet en måde at 3D-udskrive indviklede midlertidige mikrostrukturer, der kan nedbrydes efter behov ved hjælp af en biokompatibel kemisk trigger. Teknikken kunne være nyttig kunne -
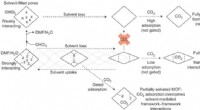 Kontinuerlig åndbar metal-organisk ramme med gæsteselektivitetForeslået rolle for gæst-ramme-interaktioner i de opløsningsmiddelafhængige kontinuerlige vejrtrækningsegenskaber af SHF-61. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2747 (Phys.org) —Forsk
Kontinuerlig åndbar metal-organisk ramme med gæsteselektivitetForeslået rolle for gæst-ramme-interaktioner i de opløsningsmiddelafhængige kontinuerlige vejrtrækningsegenskaber af SHF-61. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2747 (Phys.org) —Forsk -
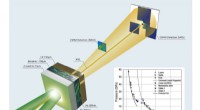 En stødinduceret mekanisme til oprettelse af organiske molekylerEksperimentel konfiguration af laserdrevne chokkomprimeringsforsøg på benzen. Kredit:Los Alamos National Laboratory Komplekse kulstofbaserede molekyler er overalt i kosmos. Hvor mange af disse mol
En stødinduceret mekanisme til oprettelse af organiske molekylerEksperimentel konfiguration af laserdrevne chokkomprimeringsforsøg på benzen. Kredit:Los Alamos National Laboratory Komplekse kulstofbaserede molekyler er overalt i kosmos. Hvor mange af disse mol
- Menneskeskabte årsager til luftforurening
- Fysikere simulerer motorolieadfærd under ekstremt tryk
- Hvorfor gav udviklingen os ikke evnen til at lugte ferskvand?
- Gratis energi er det minimum, der er nødvendigt for, at produktet dannes?
- Interaktiv teknologi kan hjælpe eleverne med at føle, hvad der ikke kan ses
- Kan der laves fodspor på månen?


