Hvad er deliquescent salte?
deliquescent salte:de "vandhungrige" forbindelser
Deliquescent -salte er stoffer, der har en stærk tilknytning til vand . Dette betyder, at de let absorberer fugt fra luften og opløses i den for at danne en flydende opløsning.
Tænk på dem som "vandhungrige" forbindelser, der er så ivrige efter at absorbere fugt, at de bliver våde på egen hånd.
Her er nogle nøgleegenskaber ved deliquescent salte:
* høj hygroskopicitet: De har en høj tendens til at tiltrække vanddamp fra atmosfæren.
* opløselighed: De er meget opløselige i vand.
* Dannelse af en løsning: Når de absorberer nok vand, opløses de fuldstændigt og danner en koncentreret opløsning.
Eksempler på deliquescent salte:
* natriumchlorid (NaCl): Dette er det almindelige bordsalt, men det er kun deliquescent under meget fugtige forhold.
* Calciumchlorid (CACL2): Brugt som et tørremiddel (tørringsmiddel) på grund af dets stærke deliquescence.
* magnesiumchlorid (MGCL2): Brugt i vejafisning og kan også bruges i brandslukkere.
* kaliumhydroxid (KOH): En stærk base, der er meget deliquescent.
* lithiumchlorid (licl): Brugt i airconditionsystemer og som tørringsmiddel.
Anvendelser af deliquescent salte:
* tørremidler: Bruges til at absorbere fugt fra luften, for eksempel i emballage for at forhindre varer i at blive fugtige.
* de-icing-agenter: Bruges til at smelte is og sne på veje og gangbroer.
* Kemiske reagenser: Brugt i forskellige kemiske processer, hvor deres stærke tilknytning til vand er fordelagtigt.
Bemærk:
* Ikke alle salte er deliquescent. Nogle salte er hygroskopiske, hvilket betyder, at de absorberer fugt, men opløses ikke nødvendigvis i den.
* Deliquescence er påvirket af faktorer som fugtighed og temperatur.
I resumé er deliquescent salte meget opløselige forbindelser med en stærk tiltrækning til vand. Deres evne til at absorbere fugt gør dem nyttige i forskellige anvendelser som tørring, afisning og kemiske reaktioner.
 Varme artikler
Varme artikler
-
 Nyt solcellemateriale kunne rense drikkevandetMed hærens finansiering har forskere ved University of Rochester udviklet et aluminiumspanel, der vinkles mod solen, renser vand. Kredit:Udlånt af University of Rochester At skaffe rent vand til s
Nyt solcellemateriale kunne rense drikkevandetMed hærens finansiering har forskere ved University of Rochester udviklet et aluminiumspanel, der vinkles mod solen, renser vand. Kredit:Udlånt af University of Rochester At skaffe rent vand til s -
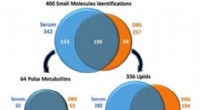 I longitudinelle undersøgelser, tørrede blodpletprøver spiller en rolleVenn -diagrammer illustrerer antallet af serum- og DBS -småmolekyleidentifikationer og overlapningen mellem prøvetyperne. De små molekyler blev adskilt i polære metabolit- og lipididentifikationer og
I longitudinelle undersøgelser, tørrede blodpletprøver spiller en rolleVenn -diagrammer illustrerer antallet af serum- og DBS -småmolekyleidentifikationer og overlapningen mellem prøvetyperne. De små molekyler blev adskilt i polære metabolit- og lipididentifikationer og -
 Sukkerovertrukket verdenGlycaner eller polysaccharider pryder celleoverflader og er vigtige for cellekommunikation, immunrespons og mange andre vitale fysiologiske processer. En ny undersøgelse samler et bibliotek af enzymer
Sukkerovertrukket verdenGlycaner eller polysaccharider pryder celleoverflader og er vigtige for cellekommunikation, immunrespons og mange andre vitale fysiologiske processer. En ny undersøgelse samler et bibliotek af enzymer -
 Forskere opdager en ny tilgang til stabilisering af katodematerialerBrookhaven -kemiker Ruoqian Lin, første forfatter til undersøgelsen. Kredit:Brookhaven National Laboratory Et team af forskere ledet af kemikere ved US Department of Energys (DOE) Brookhaven Natio
Forskere opdager en ny tilgang til stabilisering af katodematerialerBrookhaven -kemiker Ruoqian Lin, første forfatter til undersøgelsen. Kredit:Brookhaven National Laboratory Et team af forskere ledet af kemikere ved US Department of Energys (DOE) Brookhaven Natio
- Forklarer den stigende temperatur ved køling af granulatgasser
- Cellulose -nanogeneratorer kunne en dag drive implanterede biomedicinske enheder
- Hvilken forbindelse er lavet af kovalente bindinger?
- Ny fiberfri enhed forenkler fripladsbaseret kvantnøglefordeling
- Bistik, forskning, der får dig til at gå "hva?" vinde Ig Nobels (Opdatering)
- Sådan beregnes overskridelses sandsynlighed


