Når brint og ilt er i overensstemmelse med vandet, hvad ville der blive overvejet?
Den kemiske reaktion
* reaktanter: Hydrogen (H₂) og ilt (O₂) er udgangsmaterialerne.
* Produkt: Vand (H₂O) er det dannede stof.
* Kemisk ligning: 2H₂ + O₂ → 2H₂O
hvad skal man overveje
1. binding: Brint- og iltatomerne danner kemiske bindinger, specifikt kovalente bindinger, for at skabe vandmolekyler. Dette involverer deling af elektroner mellem atomerne.
2. Energiændring: Dannelsen af vand fra brint og ilt frigiver en betydelig mængde energi, hvilket gør det til en eksoterm reaktion. Dette er grunden til at brænde brint i luft (som indeholder ilt) producerer en flamme.
3. bevarelse af masse: Den samlede masse af reaktanterne (brint og ilt) er lig med den samlede masse af produktet (vand). Dette følger loven om bevarelse af masse.
4. Stater for stof: Reaktionen kan forekomme i forskellige stoftilstande:
* gas: Hydrogen- og iltgasser kombineres for at danne vanddamp.
* væske: Vanddampen kan kondensere til flydende vand.
* fast: Ved lave nok temperaturer kan vand fryse til is.
5. reversibilitet: Reaktionen kan vendes under visse betingelser (elektrolyse), hvor vand kan opdeles i brint og ilt.
Sammenfattende, når brint og ilt kombineres for at danne vand, skal du overveje den kemiske binding, energiændringer, bevarelse af masse, stoftilstande og reversibilitet af reaktionen.
Sidste artikelEr en kogt æg kemisk ændring?
Næste artikelMineral, der er højere koncentrationer i hårdt vand end blødt vand?
 Varme artikler
Varme artikler
-
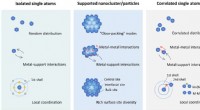 Nye elektrokatalysatorer varsler kulstofneutralitetC-SACer med metal-metal interaktioner. Sammenligning af C-SACer med de konventionelle isolerede SACer og understøttede metalliske klynge/nanopartikelkatalysatorer fra perspektivet af rumlig fordeling,
Nye elektrokatalysatorer varsler kulstofneutralitetC-SACer med metal-metal interaktioner. Sammenligning af C-SACer med de konventionelle isolerede SACer og understøttede metalliske klynge/nanopartikelkatalysatorer fra perspektivet af rumlig fordeling, -
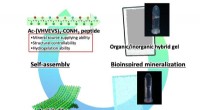 Bioinspireret mineralisering af calciumcarbonat i peptidhydrogelBioinspireret mineralisering. Kredit:Kazuki Murai et al., Journal of Asian Ceramic Societies, Taylor og Francis Et team af forskere har udviklet en biomimetisk mineralisering af calciumcarbonat ve
Bioinspireret mineralisering af calciumcarbonat i peptidhydrogelBioinspireret mineralisering. Kredit:Kazuki Murai et al., Journal of Asian Ceramic Societies, Taylor og Francis Et team af forskere har udviklet en biomimetisk mineralisering af calciumcarbonat ve -
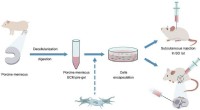 Forskere udvikler injicerbare ekstracellulære matrix-baserede biomaterialer til meniskreparationSkematisk diagram af injicerbar ECM-hydrogel til levering af BMSCer. Kredit:SIAT Menisken er et tyndt lag af bindevæv i menneskelige knæ, der hjælper med at opretholde stabiliteten af led og udf
Forskere udvikler injicerbare ekstracellulære matrix-baserede biomaterialer til meniskreparationSkematisk diagram af injicerbar ECM-hydrogel til levering af BMSCer. Kredit:SIAT Menisken er et tyndt lag af bindevæv i menneskelige knæ, der hjælper med at opretholde stabiliteten af led og udf -
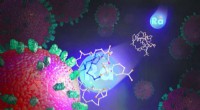 Udforsker radiums kemi for at fremme kræftbehandlinger ved hjælp af ioniserende strålingForskere ved Oak Ridge National Laboratory undersøgte radiums kemi for at få nøgleindsigt i at fremme kræftbehandlinger ved hjælp af strålebehandling. Kredit:Adam Malin/ORNL, U.S. Dept. of Energy F
Udforsker radiums kemi for at fremme kræftbehandlinger ved hjælp af ioniserende strålingForskere ved Oak Ridge National Laboratory undersøgte radiums kemi for at få nøgleindsigt i at fremme kræftbehandlinger ved hjælp af strålebehandling. Kredit:Adam Malin/ORNL, U.S. Dept. of Energy F
- Er bly en allotrop af kulstof?
- Hvad er en måde, folk kan bevare naturressourcer på?
- Kampen for at trække stikket ud:hvorfor Kiwier finder det så svært at afbryde forbindelsen til in…
- Tøjudlejning kan være nøglen til en stilfuldt bæredygtig modeindustri
- Effektiv produktion af optiske Schrödingers kattestater i stor størrelse
- Hvilken proteinfiber bruges til cellulær bevægelse og er ekstremt tynde i størrelse?


