Hvor mange gram NH3 kan produceres fra 2,63 mol N2 og overskydende H2?
1. Afbalanceret kemisk ligning:
Den afbalancerede kemiske ligning til reaktion af nitrogen og brint til dannelse af ammoniak er:
N₂ (G) + 3H₂ (G) → 2NH₃ (G)
2. Molforhold:
Den afbalancerede ligning fortæller os, at 1 mol N₂ reagerer på at producere 2 mol NH₃.
3. Beregn mol af NH₃:
Da vi har 2,63 mol N₂, kan vi bruge molforholdet til at beregne molen af NH₃ produceret:
2,63 mol N₂ × (2 mol NH₃ / 1 mol N₂) =5,26 mol NH₃
4. Konverter mol til gram:
Den molære masse af NH₃ er 17,03 g/mol. Multiplicer molen af NH₃ med dens molære masse for at finde gram:
5,26 mol nh₃ × (17,03 g nh₃ / 1 mol nh₃) = 89,6 g nh₃
Derfor kan 89,6 gram NH₃ produceres fra 2,63 mol N₂ og overskydende h₂.
 Varme artikler
Varme artikler
-
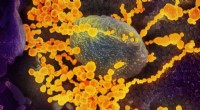 Forskere viser, at selvsteriliserende polymerer virker mod SARS-CoV-2Dette scanningselektronmikroskopbillede viser SARS-CoV-2 (runde guldobjekter), der dukker op fra overfladen af celler dyrket i laboratoriet. Kredit:NIAID-RML Forskere fra North Carolina State Un
Forskere viser, at selvsteriliserende polymerer virker mod SARS-CoV-2Dette scanningselektronmikroskopbillede viser SARS-CoV-2 (runde guldobjekter), der dukker op fra overfladen af celler dyrket i laboratoriet. Kredit:NIAID-RML Forskere fra North Carolina State Un -
 Forskere kommer op med nanobeton til støbning under negative temperaturforholdEt nærbillede af kæmpe stilladser på byggepladsen til bygning af det nye Kommunebibliotek. Til venstre er de tykke lag af stilladser nødvendige for at understøtte den forreste vandrette frontfacade. K
Forskere kommer op med nanobeton til støbning under negative temperaturforholdEt nærbillede af kæmpe stilladser på byggepladsen til bygning af det nye Kommunebibliotek. Til venstre er de tykke lag af stilladser nødvendige for at understøtte den forreste vandrette frontfacade. K -
 Gammelt brød bliver til nye tekstilerKredit:Borås Universitet Er det muligt at lave tekstiler af gammelt brød? Akram Zamani, universitetslektor i ressourcegenvinding ved universitetet i Borås, vil finde ud af det. Og hun er allerede
Gammelt brød bliver til nye tekstilerKredit:Borås Universitet Er det muligt at lave tekstiler af gammelt brød? Akram Zamani, universitetslektor i ressourcegenvinding ved universitetet i Borås, vil finde ud af det. Og hun er allerede -
 At adsorbere eller at ikke adsorbere? Det er spørgsmåletEffektiviteten af sidste-chance-terapi til patienter, der er inficeret med lægemiddelresistente bakterier, afhænger af vira, der er specialiseret i at bekæmpe dem. I modsætning, deres levedygtighed
At adsorbere eller at ikke adsorbere? Det er spørgsmåletEffektiviteten af sidste-chance-terapi til patienter, der er inficeret med lægemiddelresistente bakterier, afhænger af vira, der er specialiseret i at bekæmpe dem. I modsætning, deres levedygtighed
- Nemme opfindelser til videnskabsprojekter
- Hvad er sammenlignende eksperimenter?
- Omfattende kig på det grundlæggende i de mest ønskværdige nanorør
- Forskere dyrker regelmæssigt bestilt nanometer-skala krystallinsk tynd film ved hjælp af porøst 3…
- Vedligeholdelse af rapsoliekvalitet
- Hvad er kemi af ibuprofen?


