Kogepunktet af vand er 100 grader Celsius, men hvorfor koger det ved 130?
* kogepunkt og pres: Kogepunktet for en væske er den temperatur, hvormed dens damptryk er lig med det omgivende atmosfæriske tryk.
* Normale forhold: Ved standard atmosfærisk tryk (1 atmosfære) koges vand ved 100 grader Celsius.
* Højere pres: Hvis du øger trykket på vandet, skal du opvarme det til en højere temperatur for at få det til at koge. Dette skyldes, at du er nødt til at hæve damptrykket af vandet for at matche det højere omgivende tryk.
Her er nogle scenarier, hvor vand kan se ud til at koge ved en højere temperatur:
* Høj højde: I højere højder er atmosfæretrykket lavere. Dette betyder, at vand koger ved en lavere temperatur end 100 grader celsius.
* trykkoger: Trykkager fungerer ved at fange damp og øge trykket inde i gryden. Dette gør det muligt for vand at nå temperaturer over dets normale kogepunkt, hvilket fører til hurtigere tilberedningstider.
Kort sagt koger vand ikke ved 130 grader Celsius, medmindre det er under signifikant højere tryk end standard atmosfæretryk.
Sidste artikelHvad hedder 2 elementer blandet sammen?
Næste artikelVarmeudvekslingen i kemiske reaktioner skyldes en ændring i?
 Varme artikler
Varme artikler
-
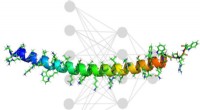 Maskinlæring opdager nye sekvenser for at booste medicinleveringMIT-forskere kombinerede eksperimentel kemi med kunstig intelligens for at opdage ikke-giftige, højaktive peptider, der kan bindes til phosphorodiamidat morpholino-oligomerer (PMO) for at hjælpe med l
Maskinlæring opdager nye sekvenser for at booste medicinleveringMIT-forskere kombinerede eksperimentel kemi med kunstig intelligens for at opdage ikke-giftige, højaktive peptider, der kan bindes til phosphorodiamidat morpholino-oligomerer (PMO) for at hjælpe med l -
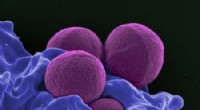 Simpel metode måler, hvor længe bakterier kan vente på antibiotikaEn farvet scanningselektronmikrograf af MRSA. Kredit:National Institute of Allergy and Infectious Diseases Et stigende antal patogener udvikler resistens over for et eller flere antibiotika, truer
Simpel metode måler, hvor længe bakterier kan vente på antibiotikaEn farvet scanningselektronmikrograf af MRSA. Kredit:National Institute of Allergy and Infectious Diseases Et stigende antal patogener udvikler resistens over for et eller flere antibiotika, truer -
 Forskere laver bæredygtig polymer af sukkerarter i træDen nye polymer er fremstillet ved hjælp af xylose, et sukker, der findes i træ. Kredit:Leszek Kobusinski Forskere fra University of Bath har lavet en bæredygtig polymer ved at bruge det næstmest
Forskere laver bæredygtig polymer af sukkerarter i træDen nye polymer er fremstillet ved hjælp af xylose, et sukker, der findes i træ. Kredit:Leszek Kobusinski Forskere fra University of Bath har lavet en bæredygtig polymer ved at bruge det næstmest -
 Stemplet, espresso, filter? Bare fordi din kaffe er bitter, betyder det ikke, at den er stærkereMoka-gryden, en anden ikonisk italiensk opfindelse, brygger kaffe ved høje temperaturer på en komfur. Kredit:Ccu.bat/Shutterstock Kaffe – en bønne med mange muligheder. Et stort valg er, hvordan ma
Stemplet, espresso, filter? Bare fordi din kaffe er bitter, betyder det ikke, at den er stærkereMoka-gryden, en anden ikonisk italiensk opfindelse, brygger kaffe ved høje temperaturer på en komfur. Kredit:Ccu.bat/Shutterstock Kaffe – en bønne med mange muligheder. Et stort valg er, hvordan ma


