Hvilket stof frigiver ioner, når de opløses i vand?
Her er hvorfor:
* ioner er atomer eller molekyler, der bærer en elektrisk ladning.
* Når en elektrolyt opløses i vand, trækker vandmolekylerne fra hinanden ionerne, der udgør elektrolytten, så de kan bevæge sig frit i opløsning.
Eksempler på elektrolytter inkluderer:
* salte: Natriumchlorid (NaCl) opløses til dannelse af natriumioner (Na+) og chloridioner (Cl-)
* syrer: Hydrochlorsyre (HCI) opløses for at danne hydrogenioner (H+) og chloridioner (Cl-)
* baser: Natriumhydroxid (NaOH) opløses til dannelse af natriumioner (Na+) og hydroxidioner (OH-)
Ikke-elektrolytter På den anden side frigør ikke ioner, når de opløstes i vand. Eksempler inkluderer sukker (saccharose) og alkohol.
Sidste artikelHvad er brydningsindeks for carbonhydrid?
Næste artikelKan ædle gasser danne forbindelser, der forekommer naturligt i miljøet?
 Varme artikler
Varme artikler
-
 Brug af kvanteprikker og en smartphone til at finde dræberbakterierForskerne Anwar Sunna (til højre) og Vinoth Kumar Rajendran med deres smartphone-aktiverede MRSA-detektor. Kredit:Sunna Lab En kombination af quantum dot nanoteknologi og et smartphonekamera kan s
Brug af kvanteprikker og en smartphone til at finde dræberbakterierForskerne Anwar Sunna (til højre) og Vinoth Kumar Rajendran med deres smartphone-aktiverede MRSA-detektor. Kredit:Sunna Lab En kombination af quantum dot nanoteknologi og et smartphonekamera kan s -
 Sundere mejeriprodukter med bakteriefilm og nanofibermembranerKredit:American Chemical Society Bakterielle biofilm er typisk målet for kraftige rengøringsregimer, men disse film er ikke altid dårlige nyheder. Faktisk, at dyrke dem på tynde plader af nanofibr
Sundere mejeriprodukter med bakteriefilm og nanofibermembranerKredit:American Chemical Society Bakterielle biofilm er typisk målet for kraftige rengøringsregimer, men disse film er ikke altid dårlige nyheder. Faktisk, at dyrke dem på tynde plader af nanofibr -
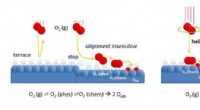 Vi forstår endelig, hvordan ilt reagerer på platinFigur til venstre:Iltmolekyler nærmer sig katalysatoroverfladen med lav hastighed. Trinene på overfladen spreder molekylerne til en svagt bundet fysisksorberet tilstand. Derfra, molekylerne kan nemt f
Vi forstår endelig, hvordan ilt reagerer på platinFigur til venstre:Iltmolekyler nærmer sig katalysatoroverfladen med lav hastighed. Trinene på overfladen spreder molekylerne til en svagt bundet fysisksorberet tilstand. Derfra, molekylerne kan nemt f -
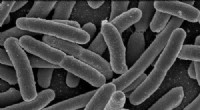 Virus skelner, ødelægge E. coli i drikkevandEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH For hurtigt at opdage tilstedeværelsen af E coli i drikkevand, Fødevareforskere fra Cornell University kan nu bruge en bakteriofa
Virus skelner, ødelægge E. coli i drikkevandEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH For hurtigt at opdage tilstedeværelsen af E coli i drikkevand, Fødevareforskere fra Cornell University kan nu bruge en bakteriofa
- Hvordan flyder energi i orientalsk medicin gennem kroppen?
- Første ICESat-2 globale data frigivet:Ice, skove og meget mere
- Koraller har et hemmeligt våben mod et opvarmet klima
- Hvordan frugtfluehjerner styrer, hvad de vælger at spise
- Hvor mange millimeter er 5 centimeter?
- De udstående T Rex-tænder? De var dækket af læber:studie


