Hvad dannes, når du blander natriumhydroxid og Epson salt sammen?
* magnesiumhydroxid (Mg (OH) ₂) :Dette er et hvidt, uopløseligt fast stof, der udfælder ud af opløsningen. Det er det, der får blandingen til at se mælkeagtig ud.
* natriumsulfat (na₂so₄) :Dette er et opløseligt salt, der forbliver opløst i opløsningen.
* vand (H₂O) :Dette produceres også i reaktionen.
Den kemiske ligning for reaktionen er:
2 NaOH (aq) + mgso₄ (aq) → mg (OH) ₂ (s) + na₂so₄ (aq)
Vigtig note: Denne reaktion er eksoterm, hvilket betyder, at den frigiver varme og kan få blandingen til at blive ret varm. Det er også vigtigt at håndtere natriumhydroxid med forsigtighed, da det er en stærk base og kan forårsage hudforbrændinger.
Her er hvad der sker mere detaljeret:
* Natriumhydroxid (NaOH) er en stærk base, der let adskiller sig i vand for at danne natriumioner (Na⁺) og hydroxidioner (OH⁻).
* Epsom salt (MGSO₄) er et opløseligt salt, der også adskiller sig i vand for at danne magnesiumioner (mg²⁺) og sulfationer (SO₄²⁻).
* Når disse ioner er i den samme opløsning, reagerer hydroxidionerne med magnesiumionerne for at danne magnesiumhydroxid (Mg (OH) ₂), som er uopløselig i vand. Derfor udfælder det ud af løsningen.
* De resterende natriumioner og sulfationer forbliver opløst i opløsningen som natriumsulfat (Na₂so₄).
Den resulterende blanding vil være en mælkeagtig hvid suspension af magnesiumhydroxid i en opløsning af natriumsulfat.
Sidste artikelHvad er ethyl- og methylalkohol, hvordan de lavede?
Næste artikelHvorfor klassificeres guld som et stof?
 Varme artikler
Varme artikler
-
 Nye salte hæver barren for lithium-ion-batteriteknologiForskere håber at gøre disse nye anioner til termisk stabile, ikke-brændbare flydende salte, hvilket gør dem gavnlige for batterier, der arbejder ved høje temperaturer. Kredit:Monash University Li
Nye salte hæver barren for lithium-ion-batteriteknologiForskere håber at gøre disse nye anioner til termisk stabile, ikke-brændbare flydende salte, hvilket gør dem gavnlige for batterier, der arbejder ved høje temperaturer. Kredit:Monash University Li -
 Ny undersøgelse af et nyligt opdaget klorofylmolekyle kan være nøglen til bedre solcellerDen detaljerede analyse af molekylet Chl f, en ny type klorofyl, som vides at spille en rolle i fotosyntesekredit:Tokyo University of Science Alle levende organismer har brug for energi for deres
Ny undersøgelse af et nyligt opdaget klorofylmolekyle kan være nøglen til bedre solcellerDen detaljerede analyse af molekylet Chl f, en ny type klorofyl, som vides at spille en rolle i fotosyntesekredit:Tokyo University of Science Alle levende organismer har brug for energi for deres -
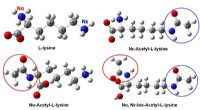 Raman og infrarød spektroskopi hjælper med at identificere forskellige acetylerede lysinerMolekylære strukturer af lysin og tre acetylerede lysiner. Kredit:Yao Guohua Et forskerhold ledet af prof. Huang Qing fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabs
Raman og infrarød spektroskopi hjælper med at identificere forskellige acetylerede lysinerMolekylære strukturer af lysin og tre acetylerede lysiner. Kredit:Yao Guohua Et forskerhold ledet af prof. Huang Qing fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabs -
 At blive kold:Fremtiden for elektronmikroskopiAndrew Minor (Kredit:Roy Kaltschmidt/Berkeley Lab) Forskere bruger elektronmikroskopi til at producere billeder i høj opløsning på atomare skala af alt fra sammensatte nanomaterialer til enkelte p
At blive kold:Fremtiden for elektronmikroskopiAndrew Minor (Kredit:Roy Kaltschmidt/Berkeley Lab) Forskere bruger elektronmikroskopi til at producere billeder i høj opløsning på atomare skala af alt fra sammensatte nanomaterialer til enkelte p
- Udøver Jorden en kraft på Merkur?
- AI kan være bedre til at detektere radarsignaler, lette frekvensdeling
- Hvorfor maling ikke tørrer langsommere i et fugtigt miljø
- Forskere viser det første 3D-billede af antistofgenet
- Best Buy udvider rækkevidden til et blomstrende sundhedsmarked med GreatCall
- Ingeniør opdager, hvorfor partikler som mel spredes på væsker


