Hvad sker der, når pH -opløsningen er lavere?
* Højere koncentration af brintioner (H+) :PH -skalaen er en logaritmisk skala, hvilket betyder, at et fald i pH med en enhed repræsenterer en ti gange stigning i hydrogenionkoncentration.
* øget surhed :En lavere pH indikerer en højere koncentration af hydrogenioner, som er ansvarlige for sure egenskaber.
* mere reaktiv :Sure opløsninger har en tendens til at være mere reaktive med andre stoffer.
* Potentiale for korrosion :Sure opløsninger kan korrodere metaller og andre materialer.
Her er nogle eksempler på, hvad der sker, når pH i en opløsning er lavere:
* mavesyre :Maven har en meget lav pH (ca. 2) på grund af tilstedeværelsen af saltsyre. Denne surhed hjælper med at fordøje mad og dræbe bakterier.
* batterisyre :Bilbatterier bruger svovlsyre, som har en meget lav pH. Denne syre giver den nødvendige kemiske energi til at drive bilen.
* regnvand :Normalt har regnvand en let sur pH (ca. 5,6) på grund af opløst kuldioxid. Imidlertid har sur regn, forårsaget af forurenende stoffer som svovldioxid og nitrogenoxider, en meget lavere pH (ca. 4 eller lavere). Dette kan skade planter, dyr og bygninger.
Husk:
* En pH på 7 er neutral.
* Værdier under 7 er sure.
* Værdier over 7 er alkaliske (grundlæggende).
Sidste artikelHvad produceres under mørke reaktioner?
Næste artikelHvordan udveksler krebsudvekslingsgas?
 Varme artikler
Varme artikler
-
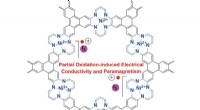 Nye 2-D metal organiske rammer med interessant elektrisk ledningsevne og magnetiske egenskaberFigur 1. Kemisk struktur af jod-dopet Ni (II) tetraaza [14] annulenbundet MOF (NiTAA-MOF). Mens NiTAA-MOF er en isolator, det oxiderede molekyle får elektrisk ledningsevne og paramagnetisme. Kredit:In
Nye 2-D metal organiske rammer med interessant elektrisk ledningsevne og magnetiske egenskaberFigur 1. Kemisk struktur af jod-dopet Ni (II) tetraaza [14] annulenbundet MOF (NiTAA-MOF). Mens NiTAA-MOF er en isolator, det oxiderede molekyle får elektrisk ledningsevne og paramagnetisme. Kredit:In -
 DNA er kun et blandt millioner af mulige genetiske molekylerKredit:CC0 Public Domain Biologi koder information i DNA og RNA, som er komplekse molekyler finjusteret til deres funktioner. Men er de den eneste måde at gemme arvelig molekylær information? Nogl
DNA er kun et blandt millioner af mulige genetiske molekylerKredit:CC0 Public Domain Biologi koder information i DNA og RNA, som er komplekse molekyler finjusteret til deres funktioner. Men er de den eneste måde at gemme arvelig molekylær information? Nogl -
 Forskere forvandler øl til brændstofKredit:CC0 Public Domain Kemikere ved University of Bristol har taget de første skridt mod at lave bæredygtig benzin ved at bruge øl som en nøgleingrediens. Det er almindeligt accepteret, at der
Forskere forvandler øl til brændstofKredit:CC0 Public Domain Kemikere ved University of Bristol har taget de første skridt mod at lave bæredygtig benzin ved at bruge øl som en nøgleingrediens. Det er almindeligt accepteret, at der -
 Nye salte hæver barren for lithium-ion-batteriteknologiForskere håber at gøre disse nye anioner til termisk stabile, ikke-brændbare flydende salte, hvilket gør dem gavnlige for batterier, der arbejder ved høje temperaturer. Kredit:Monash University Li
Nye salte hæver barren for lithium-ion-batteriteknologiForskere håber at gøre disse nye anioner til termisk stabile, ikke-brændbare flydende salte, hvilket gør dem gavnlige for batterier, der arbejder ved høje temperaturer. Kredit:Monash University Li
- Er trykket fra gas et resultat af idealloven?
- Mikrober rejser gennem luften; det ville være godt at vide hvordan og hvor
- NASA ser den tiende tropiske depression dannes i det nordvestlige Stillehav, Guam sender advarsler
- Forskellene mellem et univers, galakse og solsystem
- Virksomheder fraråder utilsigtet forskellige ideer, finder undersøgelse
- NASAs Bradford Smith, rejseleder til Voyager-missioner, dør


