Hvad er balance ligning for anilin med phenolphthalein -indikator?
Her er hvorfor:
* anilin er en svag base: Det kan acceptere en proton (H+) til at danne dens konjugatsyre, men det er ikke en stærk nok base til at få phenolphthalein til at ændre farve.
* phenolphthalein er en syre-base-indikator: Det ændrer farve baseret på pH i opløsningen. I sure opløsninger er det farveløst. I grundlæggende løsninger bliver det lyserødt.
* Ingen reaktion opstår: Anilin har ikke en betydelig indflydelse på pH i opløsningen, så phenolphthalein vil forblive farveløs i sin nærvær.
For at se en farveændring med phenolphthalein skal du tilføje en stærk base som natriumhydroxid (NaOH). Reaktionen ville se sådan ud:
NaOH (aq) + Hin (aq) ⇌ NAIN (aq) + H2O (l)
* Hin repræsenterer den farveløse form af phenolphthalein.
* Nain repræsenterer den lyserøde form af phenolphthalein.
Kortfattet:
* Anilin og phenolphthalein reagerer ikke.
* Phenolphthaleins farveændring skyldes dens interaktion med stærke baser, ikke svage baser som anilin.
Sidste artikelHvad hedder teorien, der beskæftiger sig med partikeladfærd i gasfase?
Næste artikelHvad er vægten af et pletstøv i kg?
 Varme artikler
Varme artikler
-
 Ingeniører forvandler plastisolator til varmelederForskere på MIT har designet en ny måde at konstruere en polymerstruktur på molekylært niveau, via kemisk dampaflejring. Dette giver mulighed for stive, bestilte kæder, kontra det rodede, spaghetti-li
Ingeniører forvandler plastisolator til varmelederForskere på MIT har designet en ny måde at konstruere en polymerstruktur på molekylært niveau, via kemisk dampaflejring. Dette giver mulighed for stive, bestilte kæder, kontra det rodede, spaghetti-li -
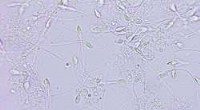 Forskere udvikler en ny clip-on-enhed til smartphones til analyse af sædcellerKredit:Lukasz Pawel Szczepanski, Shutterstock Mandlig infertilitetstest udføres i øjeblikket udelukkende i laboratorier, kræver flere besøg og flere dage for at få et resultat. Det EU-finansierede
Forskere udvikler en ny clip-on-enhed til smartphones til analyse af sædcellerKredit:Lukasz Pawel Szczepanski, Shutterstock Mandlig infertilitetstest udføres i øjeblikket udelukkende i laboratorier, kræver flere besøg og flere dage for at få et resultat. Det EU-finansierede -
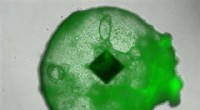 Forskere bruger RFID -chips til at spore biologiske prøverEn menneskelig leverorganoid med en indlejret RFID-mikrochip. Kredit:Kimura et al./iScience Radio frequency identification (RFID) chips bruges i dag til alt fra betaling for offentlig transport ti
Forskere bruger RFID -chips til at spore biologiske prøverEn menneskelig leverorganoid med en indlejret RFID-mikrochip. Kredit:Kimura et al./iScience Radio frequency identification (RFID) chips bruges i dag til alt fra betaling for offentlig transport ti -
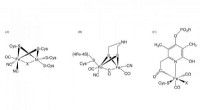 CO-biosyntese påkrævet til samling af det aktive sted i NiFe-hydrogenaseFigur 1. Struktur af de aktive steder i [NiFe] -hydrogenase, [FeFe] -hydrogenase, og [Fe] -hydrogenase Kredit:NINS/IMS En forskergruppe, der omfatter forskere fra Exploratory Research Center on Li
CO-biosyntese påkrævet til samling af det aktive sted i NiFe-hydrogenaseFigur 1. Struktur af de aktive steder i [NiFe] -hydrogenase, [FeFe] -hydrogenase, og [Fe] -hydrogenase Kredit:NINS/IMS En forskergruppe, der omfatter forskere fra Exploratory Research Center on Li
- Gamle anvendelser af svovl
- Kulstofudligninger har vidtrækkende miljømæssige fordele
- Billeddannelse af en galaksers molekylære udstrømning
- Forskere:Retssystemet skal vise mere medfølelse over for overlevende efter seksuelt misbrug
- Hvilke former, når magma tvinger sig selv på tværs af klippelag?
- Hvad er en endogen reaktion?


