Påvirker salt smeltningen af is eller ej?
* sænkning af frysepunktet: Salt sænker vandets frysepunkt. Dette betyder, at en salt vandopløsning skal være koldere end rent vand for at fryse.
* hvordan det fungerer: Når salt tilsættes til is, opløses det i det tynde vandlag, der naturligt dannes på overfladen. Dette opløste salt forstyrrer dannelsen af den krystalstruktur, som is har brug for for at forblive frosset. Saltionerne kommer i det væsentlige i vejen, hvilket gør det sværere for vandmolekyler at danne det stabile isgitter.
* Praktiske applikationer: Dette princip bruges til at smelte is på veje og fortove om vinteren. Salt sænker vandets frysepunkt og forhindrer det i at affrie, selvom temperaturen er under frysepunktet.
Vigtig note: Mens salt smelter is, får det ikke nødvendigvis til at forsvinde. Saltet opløses faktisk i vandet og skaber en salt opløsning. Denne opløsning kan derefter fryse igen, hvis temperaturen falder lavt nok, skønt frysepunktet vil være lavere end rent vand.
 Varme artikler
Varme artikler
-
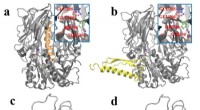 Nye glukagonlignende peptid-1-lægemidler designet til type 2-diabetesMolekylær docking mellem GLP-1-analoger og GLP-1-receptor og DPP-4. Kredit:Wang Peng Nye glukagon-lignende peptid-1 (GLP-1) lægemidler blev designet og industrielt fremstillet af forskere ved Hefei
Nye glukagonlignende peptid-1-lægemidler designet til type 2-diabetesMolekylær docking mellem GLP-1-analoger og GLP-1-receptor og DPP-4. Kredit:Wang Peng Nye glukagon-lignende peptid-1 (GLP-1) lægemidler blev designet og industrielt fremstillet af forskere ved Hefei -
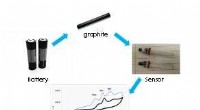 Fra batterispild til elektrokemisk sensorLabfabrikeret grafitstangsensor fra batteriaffald. Kredit:Dr. Khor Sook Mei Multiplex påvisning af antioxidanter / fødevaretilsætningsstoffer / konserveringsmidler i fødevareprøver er mulig ved hj
Fra batterispild til elektrokemisk sensorLabfabrikeret grafitstangsensor fra batteriaffald. Kredit:Dr. Khor Sook Mei Multiplex påvisning af antioxidanter / fødevaretilsætningsstoffer / konserveringsmidler i fødevareprøver er mulig ved hj -
 Belægning til metaller heler hurtigt over ridser og skrammer for at forhindre korrosionKredit:CC0 Public Domain Det er svært at tro, at en lille revne kan nedbryde en gigantisk metalkonstruktion. Men nogle gange falder broer sammen, rørledninger går i stykker og skrog løsner sig fra
Belægning til metaller heler hurtigt over ridser og skrammer for at forhindre korrosionKredit:CC0 Public Domain Det er svært at tro, at en lille revne kan nedbryde en gigantisk metalkonstruktion. Men nogle gange falder broer sammen, rørledninger går i stykker og skrog løsner sig fra -
 Gør blyrør sikreKort påføring af elektricitet på et blyrør muliggør hurtigt en sikker belægning inde i røret. Kredit:Gabriel Lobo Udvaskning af bly fra rør ind i vandforsyningen er en alvorlig bekymring for folke
Gør blyrør sikreKort påføring af elektricitet på et blyrør muliggør hurtigt en sikker belægning inde i røret. Kredit:Gabriel Lobo Udvaskning af bly fra rør ind i vandforsyningen er en alvorlig bekymring for folke
- SpaceX afbryder lanceringen efter ulige raketmotoradfærd
- Hvordan repræsenterer videnskabsmænd elementerne?
- Hvad sker der med økosystemet, når en rovdyrart er udtrykt?
- Den store korridor på Silkevejen er allerede hjemsted for højbjerghyrder over 4, 000 år siden
- Hvilke ioner er til stede i en opløsning af salpetersyre?
- Skalerbare prognoser for IoT i skyen


