Hvad er ikke -begrænsende reaktant Forklar med et passende eksempel?
Den ikke-begrænsende reaktant:den, der fortsætter med at give
I en kemisk reaktion er begrænsende reaktant er den, der først bliver brugt helt op, hvilket begrænser mængden af produkt, der kan dannes. ikke-begrænsende reaktant på den anden side er den, der er tilbage, efter at reaktionen er afsluttet.
Tænk på det som at bage en kage:
* mel er din begrænsende reaktant. Hvis du løber tør for mel, kan du ikke lave mere kage, uanset hvor meget sukker eller æg du har tilbage.
* sukker er din ikke-begrænsende reaktant. Du har måske en masse sukkerrester, men du kan ikke lave mere kage uden mel.
her er et kemisk eksempel:
Forestil dig, at vi reagerer brint (H2) og ilt (O2) at danne vand (H2O) :
2 H2 + O2 → 2 H2O
Lad os sige, at vi starter med 2 mol brint og 1 mol ilt.
* brint (H2) er den begrænsende reaktant: Dette skyldes, at reaktionen har brug for 2 mol brint for hver 1 mol ilt. Da vi kun har 1 mol ilt, kan vi kun bruge 2 mol brint til at reagere fuldt ud med det tilgængelige ilt.
* ilt (O2) er den ikke-begrænsende reaktant: Vi har 0,5 mol ilt tilbage, efter at alt brint er brugt op.
Key Takeaway:
Den ikke-begrænsende reaktant er som de ekstra ingredienser, du har tilbage efter en reaktion. Selvom det er vigtigt for reaktionen at forekomme, bestemmer det ikke, hvor meget produkt der dannes. Mængden af produkt bestemmes udelukkende af mængden af den begrænsende reaktant.
Hvorfor det betyder noget:
At forstå den begrænsende reaktant er afgørende i kemi, fordi det hjælper os:
* Beregn det teoretiske udbytte af en reaktion
* Bestem, hvor meget produkt der kan dannes fra et givet sæt reaktanter
* Optimer kemiske reaktioner ved at sikre, at alle reaktanter bruges effektivt
Kort sagt er den ikke-begrænsende reaktant den, der ikke kontrollerer reaktionens resultat, men det er stadig en vigtig komponent i processen.
 Varme artikler
Varme artikler
-
 Hydrogenbrændstoffer raketter, men hvad med strøm til dagligdagen? Var ved at komme tættere påNASA har lanceret alle sine rumfærgemissioner med brint som brændstof. Kredit:NASA, CC BY Brint er det første grundstof i det periodiske system. I sin rene form er hydrogen et lys, farveløs gas, m
Hydrogenbrændstoffer raketter, men hvad med strøm til dagligdagen? Var ved at komme tættere påNASA har lanceret alle sine rumfærgemissioner med brint som brændstof. Kredit:NASA, CC BY Brint er det første grundstof i det periodiske system. I sin rene form er hydrogen et lys, farveløs gas, m -
 Når menneskelig ekspertise forbedrer maskinernes arbejdeGeorgia Tech Ph.D. Kandidat Lee Griffin placerer enkeltkrystalprøven på måletrinnet af det modificerede atomkraftmikroskop (dvs. piezoresponskraftmikroskop). Kredit:Rob Felt, Georgia Tech Maskinlæ
Når menneskelig ekspertise forbedrer maskinernes arbejdeGeorgia Tech Ph.D. Kandidat Lee Griffin placerer enkeltkrystalprøven på måletrinnet af det modificerede atomkraftmikroskop (dvs. piezoresponskraftmikroskop). Kredit:Rob Felt, Georgia Tech Maskinlæ -
 Diætfedt interagerer med druetanniner for at påvirke vinsmagKredit:CC0 Public Domain Vinelskere erkender, at en perfekt parret vin kan få et lækkert måltid til at smage endnu bedre, men det omvendte er også sandt:Visse fødevarer kan påvirke smagen af vin
Diætfedt interagerer med druetanniner for at påvirke vinsmagKredit:CC0 Public Domain Vinelskere erkender, at en perfekt parret vin kan få et lækkert måltid til at smage endnu bedre, men det omvendte er også sandt:Visse fødevarer kan påvirke smagen af vin -
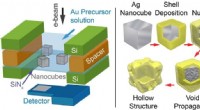 Realtidsbillede af kemiske processer(Venstre) Figur viser en skematisk af in situ LC-TEM opsætningen involverer sølv (Ag) nanokuber i en opløsning af guld (Au) ioner. (Til højre) Mekanisme, der viser den strukturelle transformation unde
Realtidsbillede af kemiske processer(Venstre) Figur viser en skematisk af in situ LC-TEM opsætningen involverer sølv (Ag) nanokuber i en opløsning af guld (Au) ioner. (Til højre) Mekanisme, der viser den strukturelle transformation unde
- Sådan fungerer atomure
- Kan revegetation returnere solcelleanlægsjord til sin uberørte herlighed?
- Ny cellemembranmodel kan være nøglen til at afdække nye proteinegenskaber
- Sådan beregnes HPLC-opløsninger
- Hvad hedder de isfrie reagioner af Antarktis?
- Hvem var den første person, der nogensinde opdagede det ydre rum?


