Hvorfor har fluor en mindre atomradius end ilt og klor?
Her er hvorfor:
* atomradius henviser til størrelsen på et neutralt atom. I dette tilfælde har fluor (F) en mindre atomradius end ilt (O) og klor (CL).
* ionisk radius henviser til størrelsen på en ion (et atom, der har vundet eller mistet elektroner). Fluor, ilt og klor danner alle negative ioner (anioner).
Hvorfor er fluorens atomradius mindre?
* Effektiv nuklearafgift: Fluor har en mindre atomradius, fordi den har en højere effektiv nuklear ladning. Dette betyder, at kernen i fluoratomet trækker stærkere på elektronerne og trækker dem tættere på kernen og gør atomet mindre.
* Antal elektronskaller: Alle tre elementer er i samme periode (række) af den periodiske tabel, hvilket betyder, at de har det samme antal elektronskaller. Fluor har imidlertid flest protoner i sin kerne, hvilket fører til en stærkere attraktion for elektronerne.
Hvorfor er fluorens ioniske radius mindre end ilt og klor?
* Elektronkonfiguration: Fluor, ilt og klor får alle elektroner til at danne deres anioner. Fluor vinder imidlertid kun en elektron, mens ilt vinder to, og klor får tre.
* Elektronafvisning: Med flere elektroner er afvisningen mellem dem større i ilt- og kloranioner, hvilket gør deres ioniske radier større.
Kortfattet:
* Fluor har en mindre atomradius end ilt og klor, fordi det har en stærkere effektiv nuklear ladning.
* Fluorens ioniske radius er mindre end ilt og klor, fordi det har færre elektroner i sin anion.
Sidste artikelEr boratomisk større eller mindre end ilt?
Næste artikelHvilket er større i størrelse aluminiumatom eller kloratom?
 Varme artikler
Varme artikler
-
 Hvor længe holder hukommelsen? Til formhukommelseslegeringer, jo længere jo bedreKredit:CC0 Public Domain Kendt for mange som muskeltråd eller memory metal, formhukommelseslegeringer er materialer, der kan bøjes eller deformeres, og derefter vende tilbage til deres oprindelige
Hvor længe holder hukommelsen? Til formhukommelseslegeringer, jo længere jo bedreKredit:CC0 Public Domain Kendt for mange som muskeltråd eller memory metal, formhukommelseslegeringer er materialer, der kan bøjes eller deformeres, og derefter vende tilbage til deres oprindelige -
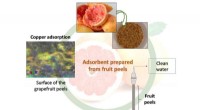 Spildevand renset takket være et nyt adsorberende materiale fremstillet af frugtskallerDiagram over processen designet af UGR-forskerne. Kredit:University of Granada Et samarbejde mellem forskere har udviklet en proces til at rense vand indeholdende tungmetaller og organiske foruren
Spildevand renset takket være et nyt adsorberende materiale fremstillet af frugtskallerDiagram over processen designet af UGR-forskerne. Kredit:University of Granada Et samarbejde mellem forskere har udviklet en proces til at rense vand indeholdende tungmetaller og organiske foruren -
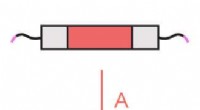 Forskere programmerer biomaterialer med logiske porte, der frigiver terapeutika som reaktion på mil…Repræsentation af en simpel JA port. De grå og orange søjler repræsenterer hele porten, som forbinder til polymererne, der holder hydrogel sammen (sorte og lilla bølgede linjer). Porten åbnes - frigiv
Forskere programmerer biomaterialer med logiske porte, der frigiver terapeutika som reaktion på mil…Repræsentation af en simpel JA port. De grå og orange søjler repræsenterer hele porten, som forbinder til polymererne, der holder hydrogel sammen (sorte og lilla bølgede linjer). Porten åbnes - frigiv -
 Omdannelse af CO2 til brugbar energiBrookhaven-forskere er afbilledet ved NSLS-II beamline 8-ID, hvor de brugte ultrastærkt røntgenlys til at se den kemiske kompleksitet af et nyt katalytisk materiale. Fra venstre mod højre ses Klaus At
Omdannelse af CO2 til brugbar energiBrookhaven-forskere er afbilledet ved NSLS-II beamline 8-ID, hvor de brugte ultrastærkt røntgenlys til at se den kemiske kompleksitet af et nyt katalytisk materiale. Fra venstre mod højre ses Klaus At
- Forskere måler en signatur af superledende interferens på atomær skala
- Skaber perfekte kanter i 2D-materialer
- Sådan smeltes en Palladium Bullion
- Undersøgelse kaster lys over, hvordan kødædende planter fik smag for kød
- Svangerskabsforebyggende smykker kunne tilbyde en ny tilgang til familieplanlægning
- Fleksibilitet på arbejdspladsen er nøglen til at hjælpe kvinder med at opretholde karriere efter …


