Ville du forvente, at Cesium Element 55 vil være mere eller mindre reaktivt end kalium?
* Elektronkonfiguration: Både cesium og kalium er i gruppe 1 i den periodiske tabel (alkalimetaller). De har en valenselektron, som de let mister for at danne en +1 -kation. Cæsium har imidlertid en større atomradius end kalium. Dette betyder, at dens valenselektron er længere væk fra kernen og oplever svagere tiltrækning til kernen.
* ioniseringsenergi: Cesium har en lavere ioniseringsenergi end kalium. Dette betyder, at det kræver mindre energi for at fjerne dets valenselektron, hvilket gør det mere sandsynligt at reagere og danne en positiv ion.
* Elektropositivitet: Cesium er mere elektropositiv end kalium. Dette betyder, at det har en større tendens til at miste elektroner og blive en kation.
Kortfattet: Cesiums større atomradius, lavere ioniseringsenergi og højere elektropositivitet bidrager alle til dens øgede reaktivitet sammenlignet med kalium.
Sidste artikelHvad er det tyngste alkaliske jord-metal?
Næste artikelHvad er atomantallet af ammonium?
 Varme artikler
Varme artikler
-
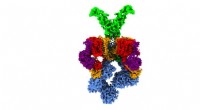 Forskere løser 3-D struktur af nanomaskine, der gør tuberkulose virulent3D-struktur af T7SS-sekretionssystemet af bakterien Mycobacterium smegmatis, svarende til den, som tuberkulosebakterien bruger under infektion. De forskellige proteiner, der udgør denne nanomaskine, e
Forskere løser 3-D struktur af nanomaskine, der gør tuberkulose virulent3D-struktur af T7SS-sekretionssystemet af bakterien Mycobacterium smegmatis, svarende til den, som tuberkulosebakterien bruger under infektion. De forskellige proteiner, der udgør denne nanomaskine, e -
 Cementfri beton slår korrosion og giver fatbergs skylEt fatberg udstillet i Melbourne Museum. Kredit:Copyright Museums Victoria, Fotograf:Rob Zugaro Forskere fra RMIT University har udviklet en miljøvenlig nul-cementbeton, hvilket næsten eliminerer
Cementfri beton slår korrosion og giver fatbergs skylEt fatberg udstillet i Melbourne Museum. Kredit:Copyright Museums Victoria, Fotograf:Rob Zugaro Forskere fra RMIT University har udviklet en miljøvenlig nul-cementbeton, hvilket næsten eliminerer -
 En overkommelig måde at opbevare ren energi påKompakte nye redoxflow-batterier til opbevaring af vedvarende energi. Kredit:Fraunhofer-Gesellschaft Vedvarende energikilder kan svinge i mængden af strøm, de er i stand til at levere - hvilket
En overkommelig måde at opbevare ren energi påKompakte nye redoxflow-batterier til opbevaring af vedvarende energi. Kredit:Fraunhofer-Gesellschaft Vedvarende energikilder kan svinge i mængden af strøm, de er i stand til at levere - hvilket -
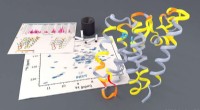 Dynamiske billeder viser rhomboid protease i aktionUndersøgelse af rhomboidproteasen GlpG ved faststof-NMR. Kredit:Barth van Rossum, FMP Rhomboide proteaser er klinisk relevante membranproteiner, der spiller en nøglerolle ved forskellige sygdomme.
Dynamiske billeder viser rhomboid protease i aktionUndersøgelse af rhomboidproteasen GlpG ved faststof-NMR. Kredit:Barth van Rossum, FMP Rhomboide proteaser er klinisk relevante membranproteiner, der spiller en nøglerolle ved forskellige sygdomme.
- Omkostningerne ved forbrugerfiber:Kan det skade at fortælle en lille hvid løgn?
- Vejledere kunne hjælpe kvindelige gymnasieelever med at slette STEM-kønsforskellen:Rapport
- Hvad er kilden til energi bag kulstofcyklus?
- Fra koraller til afgrøder:Hvordan livet beskytter planerne for dets cellulære kraftværker
- 3 udbrud af Alaska-vulkaner, der spytter lava- eller askeskyer
- Hvordan er det, at andre næringsstoffer kan metaboliseres for at give ATP?


