Forskere løser 3-D struktur af nanomaskine, der gør tuberkulose virulent
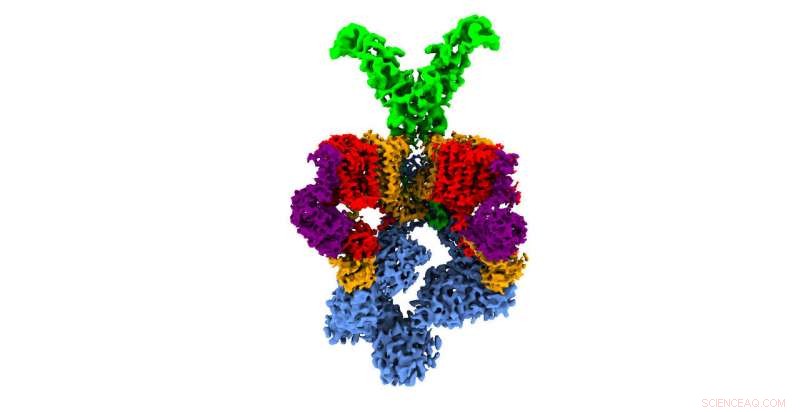
3D-struktur af T7SS-sekretionssystemet af bakterien 'Mycobacterium smegmatis', svarende til den, som tuberkulosebakterien bruger under infektion. De forskellige proteiner, der udgør denne nanomaskine, er vist i forskellige farver. I blåt, elementer af systemet, der er placeret inde i bakterien, er ansvarlige for at fange de virulensfaktorer, der produceres af bakterien, og give den nødvendige energi til deres sekretion. I grønt, del af systemet placeret uden for bakteriens membran, og det udgør en del af den pore, hvorigennem virulensfaktorer udskilles. Kredit:CNIO
Et internationalt hold ledet af Óscar Llorca ved det spanske nationale kræftforskningscenter (CNIO), og gruppen ledet af Sebastian Geibel ved universitetet i Würzburg (Tyskland), rapportere en nøjagtig 3-D-model af den mekanisme, der bruges af bakterien Mycobacterium tuberculosis til at blokere immunresponset, når man inficerer en organisme.
Dette længe ventede fund er offentliggjort i Natur . I en tid, hvor bakterier i stigende grad udvikler resistens over for antibiotika, En ende på tuberkuloseepidemien er et af de mest presserende sundhedsspørgsmål i de bæredygtige udviklingsmål, som er fastsat af FN's organisation (FN) for år 2030.
Tuberkulose er en infektionssygdom med høj dødelighed:Det er en af de 10 største dødsårsager på verdensplan, og rammer især mennesker med AIDS og andre immundefekter. Ifølge data fra WHO, 10 millioner mennesker fik tuberkulose i 2017 på verdensplan, og 1,6 mio. døde. Da den nuværende behandling har været i brug i 40 år, og nye antibiotika-resistente stammer af sygdommen dukker op, behovet for nye terapeutiske strategier er presserende.
Bakterier mod immunsystemet
Når en organisme er inficeret med M. tuberculosis, immunsystemet lancerer en kompleks reaktion for at ødelægge det. Bakterien har udviklet flere sofistikerede mekanismer til at underminere immunsystemet. Bakterien bruger et sekretionssystem - et proteinkompleks placeret i dens membran - til at injicere visse virulensfaktorer i immunsystemets celler. Disse faktorer er molekyler, der lammer immuncellernes defensive respons, så bakterier har frie tøjler til at fortsætte med at inficere kroppen.
M. tuberculosis sekretionssystemets struktur og funktionsmekanisme, kaldet T7SS (type VII sekretionssystem), ikke var blevet undersøgt i detaljer. Indtil nu, kun strukturel information i meget lav opløsning var blevet opnået, som viste en struktur i form af en hexamer (sekstakket stjerne), hvis centrum fungerer som en kanal, hvorigennem bakterien udstøder virulensfaktorerne. Manglen på information om T7SS og om hvordan det virker på atomniveau har forhindret fremskridt i at opnå nye terapeutiske strategier mod tuberkulose baseret på angreb på sekretionssystemet.
Nu, forskere Óscar Llorca og Ángel Rivera-Calzada fra CNIO, som bidrog med deres ekspertise inden for kryo-elektronmikroskopi (cryo-EM) og digital billedbehandling, og Sebastian Geibel og Nikolaos Famelis fra universitetet i Würzburg, eksperter i bakterielle sekretionssystemer, kombinerede kræfter for at løse dette puslespil. De har nu beskrevet T7SS på atomniveau. Forskerne arbejdede med en meget lignende bakterie, M. smegmatis, som bruges i forskningen som model til at studere M. tuberculosis og som deler det samme sekretionssystem med det. Arbejdet har vist, at T7SS er en sofistikeret nanomaskine, hvor flere proteiner samarbejder om at injicere de virulensfaktorer, som bakterien producerer, i immunsystemets celler.
På vej mod en ny generation af stoffer
Den seneste udvikling har forvandlet cryo-EM til en ekstremt kraftfuld teknologi, der tillader billeddannelse af molekylære strukturer i høj opløsning. Denne teknik fremskynder opnåelsen af strukturel information, som ellers ville kræve store mængder af prøven eller dens krystallisation. Med denne teknik, molekylærbiologi og biomedicin tager et stort kvalitativt spring, der forventes at revolutionere udviklingen af behandlinger af sygdomme.
I denne avis, forskerne har udpeget alle komponenterne i T7SS, og belyst funktionen af nogle af dem, der forblev ukendte. De har også modelleret dens tredimensionelle struktur og foreslået en driftsmekanisme.
"Vi var i stand til at se, at de komponenter, der indtil nu fremstod slørede med andre teknikker, er, faktisk, elementer, der er i konstant bevægelse, " forklarer Llorca. "Således, vi så, at hexameren af T7SS er sammensat af et subkompleks af 4 proteiner, og at 6 identiske kopier af dette subkompleks er nødvendige for at forme den sekstakkede stjerne omkring en central pore, hvorigennem de virulensfaktorer, der blokerer den defensive reaktion fra den inficerede organisme, udstødes." Efterfølgende, den foreslåede mekanisme blev testet af Würzburg University-gruppen ved hjælp af muterede versioner af systemet.
Det system, som den tyske gruppe bruger til at teste mekanismen, er også af stor interesse for forskersamfundet. "Det vil være meget nyttigt at teste effekten af nye molekyler rettet mod denne sekretionsmekanisme, som bakterierne af slægten Mycobacterium har brug for for at kunne udføre infektionen, " forklarer Rivera-Calzada.
Denne tværfaglige undersøgelse åbner et nyt felt for at udforske sygdomme forårsaget af bakterielle infektioner, da kendskab til de tredimensionelle strukturer af bakterielle sekretionssystemer vil gøre det muligt at udforske nye forbindelser, der blokerer sekretion. I de næste trin af denne forskning, teamet fra CNIO og universitetet i Würzburg vil forsøge at studere mere i dybden, hvordan sekretionsprocessen foregår i Mycobacterium for at åbne vejen for design af molekyler, der kan blokere den.
Sidste artikelNobelugen fortsætter med Kemiprisen
Næste artikelNy produktionsteknik til højtydende polymer kunne give bedre rustning
 Varme artikler
Varme artikler
-
 Hvordan virker gekkotape?En gekkofod og en rulle gekkotape. Kredit:Bjørn Christian Tørrissen For at løse praktiske problemer, nogle gange er alt, hvad vi skal gøre, at studere naturen. Et ofte citeret eksempel er gekkoen,
Hvordan virker gekkotape?En gekkofod og en rulle gekkotape. Kredit:Bjørn Christian Tørrissen For at løse praktiske problemer, nogle gange er alt, hvad vi skal gøre, at studere naturen. Et ofte citeret eksempel er gekkoen, -
 Kunstigt celledesign får et løft med lanceringen af FABRICELLKredit:Imperial College London FABRICELL, et fælles initiativ mellem Imperial og Kings College London, lanceret i denne måned med en række foredrag, herunder en nobelprisvinder. FABRICELL er et v
Kunstigt celledesign får et løft med lanceringen af FABRICELLKredit:Imperial College London FABRICELL, et fælles initiativ mellem Imperial og Kings College London, lanceret i denne måned med en række foredrag, herunder en nobelprisvinder. FABRICELL er et v -
 Intense test afslører undvigende, kompleks form for fælles elementForskere har genskabt en undvigende form for nitrogen ved hjælp af en højtryks ambolt med diamantspids til at presse små mængder af grundstoffet ved et tryk, der er en halv million gange så meget som
Intense test afslører undvigende, kompleks form for fælles elementForskere har genskabt en undvigende form for nitrogen ved hjælp af en højtryks ambolt med diamantspids til at presse små mængder af grundstoffet ved et tryk, der er en halv million gange så meget som -
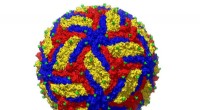 Det mest præcise billede af Zika skaber endnu potentiale for terapiDette billede i høj opløsning viser strukturen af Zika -virus. De tre konvolutglykoproteiner (E) er farvet i gult, blå og rød, og glycan er farvet i grønt. Kredit:Sevvana et al. Forskere har ska
Det mest præcise billede af Zika skaber endnu potentiale for terapiDette billede i høj opløsning viser strukturen af Zika -virus. De tre konvolutglykoproteiner (E) er farvet i gult, blå og rød, og glycan er farvet i grønt. Kredit:Sevvana et al. Forskere har ska
- 3D nano-blæk flytter branchegrænser
- Hvordan forskere bruger den internationale rumstation til at studere jordens klima
- Inspirerende opdagelse af nye lægemidler med pseudo-naturprodukter
- En bedre måde at bygge DNA-stilladser på
- Ny forskning afslører, at kreditvurderingsbureauer reagerede for langsomt på COVID-19
- Kunne vakuumfysikken afsløres af laserdrevne mikrobobler?


