Reagerer cupric chlorid med Mg?
Her er den afbalancerede kemiske ligning:
cucl₂ (aq) + mg (s) → mgcl₂ (aq) + cu (s)
Forklaring:
* magnesium (mg) er mere reaktiv end kobber (CU) . Dette betyder, at det kan fortrænge kobber fra dets forbindelse.
* I reaktionen mister magnesiumatomer to elektroner hver og bliver magnesiumioner (mg²⁺) .
* Kobberioner (cu²⁺) fra cupric chlorid får to elektroner hver, bliver kobberatomer (Cu) .
* Magnesiumionerne kombineres derefter med chloridioner (CL⁻) for at danne magnesiumchlorid (MGCL₂) , som er opløselig i vand.
Observationer:
* Du vil observere et rødbrunt fast stof (kobber), der dannes på overfladen af magnesiummetal.
* Opløsningen vil sandsynligvis blive fra blå (på grund af tilstedeværelsen af Cu²⁺ -ioner) til farveløs (på grund af tilstedeværelsen af mg²⁺ioner).
* Reaktionen kan producere varme, hvilket indikerer en eksoterm reaktion.
Bemærk: Reaktionen fortsætter lettere, hvis magnesiumet er i en pulverform, eller hvis opløsningen opvarmes.
 Varme artikler
Varme artikler
-
 Porøse materialer måler temperatur på molekylært niveauKredit:CC0 Public Domain Forskere fra Gent Universitet undersøgte, hvordan såkaldte metal-organiske rammer ånder, når det bliver varmere eller koldere. Ved hjælp af avancerede computersimuleringer
Porøse materialer måler temperatur på molekylært niveauKredit:CC0 Public Domain Forskere fra Gent Universitet undersøgte, hvordan såkaldte metal-organiske rammer ånder, når det bliver varmere eller koldere. Ved hjælp af avancerede computersimuleringer -
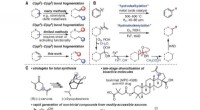 En mere effektiv måde at spalte vedhængende olefiner fra terpener og lignende forbindelserKoncept og anvendelser af hydrodealkenylativ fragmentering af C(sp 3 )–C(sp 2 ) obligationer. (A) Dekonstruktiv fragmentering af C-C-bindinger. (B) Oversigt og foreslået mekanisme for hydrodealken
En mere effektiv måde at spalte vedhængende olefiner fra terpener og lignende forbindelserKoncept og anvendelser af hydrodealkenylativ fragmentering af C(sp 3 )–C(sp 2 ) obligationer. (A) Dekonstruktiv fragmentering af C-C-bindinger. (B) Oversigt og foreslået mekanisme for hydrodealken -
 Nye molekylære prober til opioidreceptorerVed hjælp af specielle ligander, det var muligt at bevise, at opioidreceptorer også er til stede som par af to i cellemembranen. Kredit:Scigraphix Stærke smertestillende midler er meget vigtige i
Nye molekylære prober til opioidreceptorerVed hjælp af specielle ligander, det var muligt at bevise, at opioidreceptorer også er til stede som par af to i cellemembranen. Kredit:Scigraphix Stærke smertestillende midler er meget vigtige i -
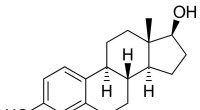 Østrogene og anti-østrogene virkninger af PFAS'er kan afhænge af tilstedeværelsen af østrogenEstradiol, det største østrogen kønshormon hos mennesker og en meget brugt medicin. Kredit:Public Domain Perfluoralkylstoffer (PFASer) har modtaget intens kontrol i de seneste år på grund af deres
Østrogene og anti-østrogene virkninger af PFAS'er kan afhænge af tilstedeværelsen af østrogenEstradiol, det største østrogen kønshormon hos mennesker og en meget brugt medicin. Kredit:Public Domain Perfluoralkylstoffer (PFASer) har modtaget intens kontrol i de seneste år på grund af deres


