Hvilke elementer ville vise lignende egenskaber som NA?
Her er grunden til, at elementer i den samme gruppe har lignende egenskaber, og nogle specifikke eksempler på elementer, der ligner natrium:
* Valenselektroner: Elementer i den samme gruppe har det samme antal valenselektroner. Disse elektroner er involveret i kemisk binding og bestemmer, hvordan et atom vil reagere med andre atomer. Da natrium har en valenselektron, har andre alkalimetaller også en valenselektron.
* Lignende reaktivitet: På grund af deres enkelt valenselektron er alkalimetaller meget reaktive. De mister let dette elektron til dannelse af en +1 ion, hvilket gør dem til gode reduktionsmidler.
* Lignende kemiske egenskaber: De reagerer på lignende måde med vand, ilt og halogener og danner lignende forbindelser.
elementer, der ligner natrium:
* lithium (Li): Det letteste alkalimetal, lithium er også meget reaktiv, men mindre end natrium.
* kalium (k): Kalium er mere reaktiv end natrium og findes ofte i gødning og elektrolytter.
* rubidium (RB): Et blødt, sølvhvidt metal, rubidium er endnu mere reaktiv end kalium.
* cesium (CS): Det mest reaktive alkalimetal, cæsium, bruges i atomur og som en getter i vakuumrør.
Key Takeaway: Elementer i den samme gruppe af den periodiske tabel deler lignende egenskaber på grund af deres lignende elektroniske konfigurationer, især antallet af valenselektroner. Derfor vil elementer i gruppe 1 (alkalimetaller) som lithium, kalium, rubidium og cæsium udvise lignende egenskaber som natrium.
 Varme artikler
Varme artikler
-
 Højopløsnings strukturel analyse af protein bag Huntingtons sygdomEn international kohorte af forskere, herunder ingeniører fra Washington University i St. Louis, for nylig visualiseret Huntingtons protein for første gang. Det er håbet, at at vide mere om strukturen
Højopløsnings strukturel analyse af protein bag Huntingtons sygdomEn international kohorte af forskere, herunder ingeniører fra Washington University i St. Louis, for nylig visualiseret Huntingtons protein for første gang. Det er håbet, at at vide mere om strukturen -
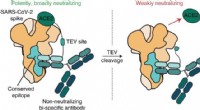 Molekylær makeover gør wimpy antistof til en SARS-CoV-2 tacklerGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01140-1 Ligesom Roadrunner, der overliste Wile E. Coyote, bliver SARS-CoV-2 (den infektiøse virus, der er ansvarlig f
Molekylær makeover gør wimpy antistof til en SARS-CoV-2 tacklerGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01140-1 Ligesom Roadrunner, der overliste Wile E. Coyote, bliver SARS-CoV-2 (den infektiøse virus, der er ansvarlig f -
 Ved at opdage genetisk materiale, hurtig sensor har potentiel anvendelse som et klinisk værktøj3D-model af DNA. Kredit:Michael Ströck/ Wikimedia/ GNU Free Documentation License På mindre end et sekund, en lille sensor, der bruges i hjernekemiforskning, kan detektere nøglemolekylerne, der gi
Ved at opdage genetisk materiale, hurtig sensor har potentiel anvendelse som et klinisk værktøj3D-model af DNA. Kredit:Michael Ströck/ Wikimedia/ GNU Free Documentation License På mindre end et sekund, en lille sensor, der bruges i hjernekemiforskning, kan detektere nøglemolekylerne, der gi -
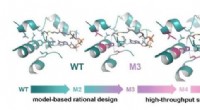 Udvidelse af grænserne for kuldioxidfikseringEngineering af glycolyl-CoA carboxylase (GCC), nøgleenzymet i TaCo-vejen. GCC blev udviklet på stilladset af en naturligt forekommende propionyl-CoA carboxylase (WT). Rationelt design førte til den 50
Udvidelse af grænserne for kuldioxidfikseringEngineering af glycolyl-CoA carboxylase (GCC), nøgleenzymet i TaCo-vejen. GCC blev udviklet på stilladset af en naturligt forekommende propionyl-CoA carboxylase (WT). Rationelt design førte til den 50
- Cassini udforsker ringlignende formationer omkring Titans søer
- Hvad krybdyrknogler kan lære os om Jordens farefulde fortid
- Supersoniske gasstrømme, der er tilovers fra Big Bang, driver massiv sorte hulformation
- Afsløring af samspillet mellem to berømte kvanteeffekter
- 3-D-print eliminerer uønskede egenskaber i konventionelle superlegeringer
- Hvordan et ballonbåret eksperiment kan gøre arbejdet med Hubble-rumteleskopet


