Hvad sker der, når natriumbromid er i vand?
* natriumioner (Na+)
* bromidioner (Br-)
Her er en sammenbrud:
1. opløsning: NABR er en opløselig ionisk forbindelse , hvilket betyder, at det har en stærk tiltrækning til vandmolekyler. Når NABR tilsættes til vand, omgiver vandmolekylerne NABR -ioner og trækker dem fra krystalgitteret.
2. dissociation: Når NABR -ionerne er adskilt fra krystalen, bliver de omgivet af vandmolekyler og danner hydrerede ioner . Denne proces kaldes dissociation , og det resulterer i dannelsen af frie Na+ og BR-ioner i opløsning.
Reaktionen kan repræsenteres af følgende ligning:
NABR (s) → Na + (aq) + Br- (aq)
hvor:
* (s) angiver et solidt
* (aq) Angiver en vandig opløsning (opløst i vand)
Nøglepunkter:
* Løsningen bliver elektrisk ledende På grund af tilstedeværelsen af frie ioner.
* Dissociation er reversibel , hvilket betyder, at nogle Na+ og BR-ioner kan omkranse til at danne NABR i opløsning. I en mættet opløsning favoriserer ligevægten imidlertid den dissocierede form.
* Den resulterende løsning er neutral , da hverken natriumioner eller bromidioner er særlig sure eller basale.
Derfor, når natriumbromid er i vand, opløses det og adskiller sig i dens komponentioner, hvilket resulterer i en klar, farveløs opløsning, der udfører elektricitet.
 Varme artikler
Varme artikler
-
 Nanopartikelsensor kan skelne mellem viral og bakteriel lungebetændelseKredit:Unsplash/CC0 Public Domain Mange forskellige typer bakterier og vira kan forårsage lungebetændelse, men der er ingen nem måde at afgøre, hvilken mikrobe der forårsager en bestemt patients sy
Nanopartikelsensor kan skelne mellem viral og bakteriel lungebetændelseKredit:Unsplash/CC0 Public Domain Mange forskellige typer bakterier og vira kan forårsage lungebetændelse, men der er ingen nem måde at afgøre, hvilken mikrobe der forårsager en bestemt patients sy -
 Simpel kemi vil øge bæredygtigheden af betonproduktionKredit:University of Tokyo Forskere ved Institut for Industrividenskab, en del af University of Tokyo, har udviklet en ny metode til fremstilling af beton uden cement. De har direkte bundet sandpa
Simpel kemi vil øge bæredygtigheden af betonproduktionKredit:University of Tokyo Forskere ved Institut for Industrividenskab, en del af University of Tokyo, har udviklet en ny metode til fremstilling af beton uden cement. De har direkte bundet sandpa -
 Teknik giver detaljeret overblik over, hvordan visse polymerer dannes, låse op for svar om kernedan…Forskningen pryder forsiden af Physical Chemistry Chemical Physics. Kredit:Royal Society of Chemistry Forestil dig en lille dråbe. Den indeholder vand, det brusende antiseptiske hydrogenperoxid,
Teknik giver detaljeret overblik over, hvordan visse polymerer dannes, låse op for svar om kernedan…Forskningen pryder forsiden af Physical Chemistry Chemical Physics. Kredit:Royal Society of Chemistry Forestil dig en lille dråbe. Den indeholder vand, det brusende antiseptiske hydrogenperoxid, -
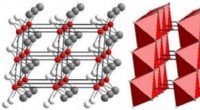 Mineralopdagelse gjort nemmere:Røntgenteknik kaster nyt lys på bittesmå, sjældne krystallerDisse diagrammer viser atomkrystalstrukturen af ognitit. Til venstre, atomer i den krystallinske struktur er repræsenteret i rødt (nikkel), hvid (tellur), og grå (vismut). Til højre, en polyhedral r
Mineralopdagelse gjort nemmere:Røntgenteknik kaster nyt lys på bittesmå, sjældne krystallerDisse diagrammer viser atomkrystalstrukturen af ognitit. Til venstre, atomer i den krystallinske struktur er repræsenteret i rødt (nikkel), hvid (tellur), og grå (vismut). Til højre, en polyhedral r
- Forskere opdager, hvordan de første kvasarer i universet blev dannet
- Forskere analyserer det første gamle menneskelige DNA fra Sydøstasien
- Dinitrogenoxidemissioner 300 gange stærkere end kuldioxid bringer Jordens fremtid i fare
- Lås op for kraften i citrin, der betyder:Helbredende egenskaber og anvendelser
- Studie:Politisk, økonomisk, sociale faktorer påvirker lokale beslutninger om dødsstraf
- Hvordan fødevaretilgængelighed kunne katalysere kulturel transmission i vilde orangutanger


