Beregn pH for en puffer dannet ved at blande 85 ml 0,13 M mælkesyre med 95 0,15 natriumlactat?
1. Forstå buffersystemet
* mælkesyre (HC3H5O3) er en svag syre.
* natriumlactat (NAC3H5O3) er salt af dets konjugatbase, laktation (C3H5O3-).
2. Brug Henderson-Hasselbalch-ligningen
PH af en pufferopløsning bestemmes af Henderson-Hasselbalch-ligningen:
pH =PKA + log ([Conjugate Base]/[Svag syre])
* pka: Den negative logaritme af syredissocieringskonstanten (KA) for mælkesyre. Du kan finde denne værdi i en tabel eller online. PKA for mælkesyre er ca. 3,86.
* [Conjugate Base]: Koncentrationen af laktationer (C3H5O3-).
* [Svag syre]: Koncentrationen af mælkesyre (HC3H5O3).
3. Beregn koncentrationerne af syre- og konjugatbasen
* mælkesyre:
* Mol mælkesyre =(0,085 L) * (0,13 mol/L) =0,01105 mol
* Koncentration af mælkesyre i pufferen =(0,01105 mol) / (0,085 L + 0,095 L) =0,0614 mol / L
* Laktation:
* Mol natriumlactat =(0,095 l) * (0,15 mol/l) =0,01425 mol
* Koncentration af laktation i bufferen =(0,01425 mol) / (0,085 L + 0,095 L) =0,0792 mol / L
4. Sæt værdierne i ligningen
pH =3,86 + log (0,0792 / 0,0614)
pH ≈ 3,86 + 0,11
pH ≈ 3,97
Derfor er pH af bufferopløsningen ca. 3,97.
 Varme artikler
Varme artikler
-
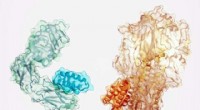 Ny metode til at generere potente, specifikke bindingsproteiner til nye lægemidlerSmå proteiner (mørkere nuance) designet til at binde sig til insulinreceptoren (venstre) og en komponent af influenzavirussen (højre). Kredit:Ian C. Haydon/Institute for Protein Design Et team af v
Ny metode til at generere potente, specifikke bindingsproteiner til nye lægemidlerSmå proteiner (mørkere nuance) designet til at binde sig til insulinreceptoren (venstre) og en komponent af influenzavirussen (højre). Kredit:Ian C. Haydon/Institute for Protein Design Et team af v -
 Rejeskaller til fremstilling af elektroder til store batterierDe spanske forskeres forslag er at producere vanadium flow batterielektroder fra kitin, et materiale fra rejeskaller. Kredit:John Cameron / Unsplash Et projekt af spanske forskere og andre samarbe
Rejeskaller til fremstilling af elektroder til store batterierDe spanske forskeres forslag er at producere vanadium flow batterielektroder fra kitin, et materiale fra rejeskaller. Kredit:John Cameron / Unsplash Et projekt af spanske forskere og andre samarbe -
 Nye værktøjer til at skabe spejlede former for molekylerGregory Fu og Zhaobin Wang hos Caltech. Kredit:Caltech En af de største udfordringer, som syntetiske kemikere står over for, er, hvordan man laver molekyler af kun en bestemt håndhævelse. Molekyle
Nye værktøjer til at skabe spejlede former for molekylerGregory Fu og Zhaobin Wang hos Caltech. Kredit:Caltech En af de største udfordringer, som syntetiske kemikere står over for, er, hvordan man laver molekyler af kun en bestemt håndhævelse. Molekyle -
 Grønnere, hurtigere og billigere måde at lave mønstrede metaller til solceller og elektronikAlle tre forskere fra venstre mod højre:Dr. Ross Hatton, Dr Silva Varagnolo og Dr. Jaemin Lee. Kredit:University of Warwick En innovativ måde at mønstre metaller er blevet opdaget af forskere ved
Grønnere, hurtigere og billigere måde at lave mønstrede metaller til solceller og elektronikAlle tre forskere fra venstre mod højre:Dr. Ross Hatton, Dr Silva Varagnolo og Dr. Jaemin Lee. Kredit:University of Warwick En innovativ måde at mønstre metaller er blevet opdaget af forskere ved


