Hvad er stærke og svage molekylære kræfter?
Stærke vs. svage molekylære kræfter
molekylære kræfter er de attraktive eller frastødende kræfter, der findes mellem molekyler. Disse kræfter bestemmer mange fysiske egenskaber ved stoffer, såsom smeltepunkt, kogepunkt og opløselighed.
Her er en sammenbrud af stærke og svage molekylære kræfter:
Stærke molekylære kræfter:
* kovalente obligationer: Dette er den stærkeste type molekylær kraft, der involverer deling af elektroner mellem atomer. De holder atomer sammen inden for et molekyle. Eksempler inkluderer bindingerne i vand (H₂O) og metan (CH₄).
* ioniske bindinger: Disse involverer den elektrostatiske tiltrækning mellem modsat ladede ioner. De er også stærke, men svagere end kovalente obligationer. Et eksempel er bindingen i natriumchlorid (NaCl).
svage molekylære kræfter:
* van der Waals Forces: Dette er svage kræfter med kort rækkevidde, der opstår fra midlertidige udsving i elektronfordeling omkring molekyler. De er yderligere opdelt i:
* London Dispersion Forces: Forekommer i alle molekyler og er til stede selv i ædelgasser. De er svagere end dipol-dipol-kræfter.
* dipol-dipol-kræfter: Forekommer mellem polære molekyler, hvor den positive ende af et molekyle tiltrækkes af den negative ende af en anden.
* Hydrogenbinding: En speciel type dipol-dipolinteraktion, der opstår, når et hydrogenatom er bundet til et meget elektronegativt atom (som ilt, nitrogen eller fluor). Dette er en relativt stærk type van der Waals Force.
Nøgleforskelle:
| Funktion | Stærke molekylære kræfter | Svage molekylære kræfter |
| ----------------- | --------------------------- | ---------------------- |
| Obligationsstyrke | Stærk | Svag |
| Interaktionstype | Inden for molekyler | Mellem molekyler |
| Eksempler | Kovalent, ionisk | Van der Waals |
| Effekt på egenskaber | Højere smeltnings-/kogepunkter, lavere damptryk | Lavere smelte/kogepunkter, højere damptryk |
Kortfattet:
* Stærke molekylære kræfter Hold atomer sammen i et molekyle og kræver betydelig energi for at bryde.
* svage molekylære kræfter er ansvarlige for samspillet mellem molekyler og kan påvirke egenskaber som kogepunkt og opløselighed.
At forstå styrken af molekylære kræfter er afgørende for at forudsige og forklare opførelsen af forskellige stoffer.
 Varme artikler
Varme artikler
-
 Forskere finder, at frøskal kunne føre til stærke, hård, men alligevel fleksible materialerKarakteristiske træk ved frøkappen af Portulaca oleracea , en årlig sukkulent almindeligvis kendt som verdolaga eller portulak. A) Foto af P. oleracea blomst , B) Fotografi af de bittesmå sorte fr
Forskere finder, at frøskal kunne føre til stærke, hård, men alligevel fleksible materialerKarakteristiske træk ved frøkappen af Portulaca oleracea , en årlig sukkulent almindeligvis kendt som verdolaga eller portulak. A) Foto af P. oleracea blomst , B) Fotografi af de bittesmå sorte fr -
 Kærlighed-had forhold mellem opløsningsmiddel og vand fører til bedre biomasseopløsningEt organisk opløsningsmiddel, vist med gult, og vand, vist i blåt, adskille og danne nanoklynger på de hydrofobe og hydrofile sektioner af grønt plantemateriale, driver den effektive dekonstruktion af
Kærlighed-had forhold mellem opløsningsmiddel og vand fører til bedre biomasseopløsningEt organisk opløsningsmiddel, vist med gult, og vand, vist i blåt, adskille og danne nanoklynger på de hydrofobe og hydrofile sektioner af grønt plantemateriale, driver den effektive dekonstruktion af -
 Havmuslinger er en model til forbedring af styrke, strækbarhed og vedhæftning i hydrogeler til så…Kredit:Pixabay/CC0 Public Domain Hydrogeler er overalt. De er vandelskende polymerer, der kan absorbere og tilbageholde vand, og kan findes i sådanne dagligdags forbrugerprodukter som bløde kontak
Havmuslinger er en model til forbedring af styrke, strækbarhed og vedhæftning i hydrogeler til så…Kredit:Pixabay/CC0 Public Domain Hydrogeler er overalt. De er vandelskende polymerer, der kan absorbere og tilbageholde vand, og kan findes i sådanne dagligdags forbrugerprodukter som bløde kontak -
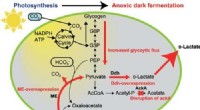 Metoden giver høj mængde af D-lactat ved hjælp af cyanobakterier, kunne revolutionere produktione…Figur 1:Vejen til omdannelse af kuldioxid til D-laktat. Synechocystis sp. PCC 6803 producerer glykogen inde i sine celler fra CO2 og lys. Det blev afsløret, at når Synechocystis sp. PCC 6803, der har
Metoden giver høj mængde af D-lactat ved hjælp af cyanobakterier, kunne revolutionere produktione…Figur 1:Vejen til omdannelse af kuldioxid til D-laktat. Synechocystis sp. PCC 6803 producerer glykogen inde i sine celler fra CO2 og lys. Det blev afsløret, at når Synechocystis sp. PCC 6803, der har
- Ansættelsesboom hos SpaceX og Blue Origin gør det svært for NASA at tiltrække talenter
- Forskere opdager massedød af havliv ud for Ruslands Kamchatka
- Billede:Proba-V passerer faklen
- Luftforurening dræber over 500, 000 europæere om året:rapport
- Kan folk lære at omfavne risiko?
- Verdensomspændende byudvidelse skaber problemer


