Hvordan fordeles elektronerne omkring atomkernen?
1. Elektronskaller:
* Elektroner besætter forskellige energiniveauer kaldet elektronskaller . Disse skaller er nummereret 1, 2, 3 osv., Med højere antal, der indikerer højere energiniveau.
* Jo længere væk en skal er fra kernen, jo højere er det energiniveau.
* Hver skal kan have et maksimalt antal elektroner:
* Shell 1:2 elektroner
* Shell 2:8 Elektroner
* Shell 3:18 elektroner
* Shell 4:32 Elektroner og så videre.
2. Underskaller:
* Hver elektronskal er yderligere opdelt i underskaller, betegnet med bogstaver:S, P, D og F.
* Underskallerne inden for en skal har lidt forskellige energiniveauer.
* s-subshell: Kan maksimalt indeholde 2 elektroner. Det er sfærisk i form.
* p-subshell: Kan maksimalt indeholde 6 elektroner. Det har en håndvægtformet form.
* d-subshell: Kan maksimalt indeholde 10 elektroner. Det har mere komplekse former.
* f-subshell: Kan maksimalt indeholde 14 elektroner. Det har endnu mere komplekse former.
3. Orbitals:
* Inden for hvert underskal er der specifikke regioner i rummet kaldet orbitaler hvor elektroner mest sandsynligt findes.
* Hver orbital kan maksimalt holde to elektroner med modsatte spins (Pauli -ekskluderingsprincip).
* Formen og antallet af orbitaler inden for et underskal afhænger af underskaletypen:
* S-subshell:1 Orbital (sfærisk)
* p-subshell:3 orbitaler (håndvægtformet)
* D-subshell:5 orbitaler (mere komplekse former)
* f-subshell:7 orbitaler (endnu mere komplekse former)
4. Elektronkonfiguration:
* elektronkonfiguration af et atom beskriver arrangementet af dets elektroner i skaller, underskaller og orbitaler.
* Det følger specifikke regler:
* Aufbau -princippet:Elektroner udfylder orbitaler i rækkefølge af stigende energi.
* Hunds regel:Elektroner vil individuelt besætte orbitaler inden for et underskal, før de fordobles i en orbital.
* Pauli -ekskluderingsprincippet:Ingen to elektroner i et atom kan have det samme sæt med fire kvantetal.
Eksempel:Carbon (c)
* Atomnummer:6, hvilket betyder, at det har 6 elektroner.
* Elektronkonfiguration:1S² 2S² 2p²
* Shell 1:2 elektroner (1S²)
* Shell 2:4 Elektroner (2S² 2p²)
* 2S-subshell:2 elektroner
* 2p-subshell:2 elektroner (en i hver af de tre p-orbitaler)
Nøglepunkter:
* Elektroner kredser ikke kernen som planeter omkring en sol.
* Elektronfordelingen er sandsynlig, hvilket betyder, at vi kun kan forudsige de mest sandsynlige placeringer af elektroner inden for specifikke rumområder.
* Forståelse af elektronkonfiguration er afgørende for at forklare kemisk binding, reaktivitet og egenskaberne ved elementer.
Fortæl mig, hvis du har yderligere spørgsmål om elektronfordelingen i atomer!
 Varme artikler
Varme artikler
-
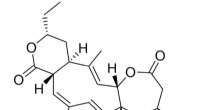 Et usædvanligt molekyle beskytter nerveceller mod degenerationDen kemiske struktur af collinolacton. Kredit:University of Tübingen Et internationalt forskerhold ledet af professor Stephanie Grond fra Institute of Organic Chemistry ved University of Tübingen
Et usædvanligt molekyle beskytter nerveceller mod degenerationDen kemiske struktur af collinolacton. Kredit:University of Tübingen Et internationalt forskerhold ledet af professor Stephanie Grond fra Institute of Organic Chemistry ved University of Tübingen -
 Forskere finder en ny anvendelse af affaldUBCO Postdoc-stipendiat Dr. Chinchu Cherian, sammen med lektor Dr. Sumi Siddiqua, undersøger et vejbygningsmateriale lavet delvist med genanvendt træaske. Kredit:UBCO Affaldsmaterialer fra papirma
Forskere finder en ny anvendelse af affaldUBCO Postdoc-stipendiat Dr. Chinchu Cherian, sammen med lektor Dr. Sumi Siddiqua, undersøger et vejbygningsmateriale lavet delvist med genanvendt træaske. Kredit:UBCO Affaldsmaterialer fra papirma -
 Kemikere opdager nye signaturer til at identificere cystisk fibrose hos spædbørn førPhilip Britz-McKibbin, Professor i Institut for Kemi og Kemisk Biologi, McMaster University. Kredit:JD Howell, McMaster University Forskere ved McMaster University har opdaget flere nye biomarkøre
Kemikere opdager nye signaturer til at identificere cystisk fibrose hos spædbørn førPhilip Britz-McKibbin, Professor i Institut for Kemi og Kemisk Biologi, McMaster University. Kredit:JD Howell, McMaster University Forskere ved McMaster University har opdaget flere nye biomarkøre -
 Brug af bakterier til at fremskynde CO2-opsamling i haveneBerkeley Lab-forsker Peter Agbo blev tildelt en bevilling til et kulstoffangstprojekt under Labs Carbon Negative Initiative. Kredit:Marilyn Sargent/Berkeley Lab Du er måske bekendt med direkte luft
Brug af bakterier til at fremskynde CO2-opsamling i haveneBerkeley Lab-forsker Peter Agbo blev tildelt en bevilling til et kulstoffangstprojekt under Labs Carbon Negative Initiative. Kredit:Marilyn Sargent/Berkeley Lab Du er måske bekendt med direkte luft
- Masser af liv fundet dybt inde i jordens overflade
- Hjemmelavede Finch Bird Feeders
- Hvad er den hastighed, hvormed olie fordamper?
- Gamle floder afslører flere grønne ørkener i Sahara
- Astronomer opdager otte begravede dobbelte AGN-kandidater
- Se små elektromekaniske robotter, der er hurtigere end geparder på grund af deres størrelse


