De elektroner, der stort set er ansvarlige for en kemisk opførsel af atomer, kaldes?
Her er hvorfor:
* valenselektroner er elektronerne i det yderste energiniveau af et atom.
* Det er dem, der interagerer med andre atomer, når de danner kemiske bindinger.
* Antallet af valenselektroner bestemmer en atoms bindingskapacitet og dens tendens til at vinde, miste eller dele elektroner.
* Dette dikterer igen de typer kemiske forbindelser, som et atom kan danne og dets samlede reaktivitet.
For eksempel:
* natrium (NA) Har en valenselektron, hvilket gør det meget reaktivt og tilbøjeligt til at miste denne elektron til at danne en positiv ion.
* klor (Cl) Har syv valenselektroner, hvilket gør det ivrig efter at få et elektron for at afslutte sin ydre skal og danne en negativ ion.
* Interaktionen mellem natrium og klor resulterer i dannelsen af natriumchlorid (NaCl), en stabil forbindelse med ioniske bindinger.
 Varme artikler
Varme artikler
-
 Hvordan man gør biokatalysatorer udødeligeNicolas Plumeré, Darren Buesen og Li Huaiguang (fra venstre). Kredit:RUB, Marquard Oxygen truer bæredygtige katalysatorer, der bruger hydrogen til at producere elektricitet i brændselsceller. Fors
Hvordan man gør biokatalysatorer udødeligeNicolas Plumeré, Darren Buesen og Li Huaiguang (fra venstre). Kredit:RUB, Marquard Oxygen truer bæredygtige katalysatorer, der bruger hydrogen til at producere elektricitet i brændselsceller. Fors -
 Li-ioner transporterer på tværs af elektrolytter og SEIKredit:CC0 Public Domain Li-ion-transportens kinetik på tværs af elektrolytten og SEI er sædvanligvis det hastighedsbestemmende trin i Li-plettering-stripningsprocessen. Før galvanisering på anode
Li-ioner transporterer på tværs af elektrolytter og SEIKredit:CC0 Public Domain Li-ion-transportens kinetik på tværs af elektrolytten og SEI er sædvanligvis det hastighedsbestemmende trin i Li-plettering-stripningsprocessen. Før galvanisering på anode -
 Fysikere opdager en tri-anion partikel med kolossal stabilitetKredit:Virginia Commonwealth University Forskere fra Virginia Commonwealth University har opnået en bedrift, der er den første inden for fysik og kemi-en der kunne have vidtrækkende anvendelser.
Fysikere opdager en tri-anion partikel med kolossal stabilitetKredit:Virginia Commonwealth University Forskere fra Virginia Commonwealth University har opnået en bedrift, der er den første inden for fysik og kemi-en der kunne have vidtrækkende anvendelser. -
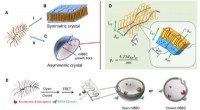 Sætter naturens krystalsymmetri på pause for at fremme målrettet medicinleveringDrexel-forskere opdagede, at pakning af flere polymer børster på en molekylær flaskebørstepolymer får den til at bøje, som er grundlaget for sfærisk krystalvækst. Kredit:Drexel University Fra snef
Sætter naturens krystalsymmetri på pause for at fremme målrettet medicinleveringDrexel-forskere opdagede, at pakning af flere polymer børster på en molekylær flaskebørstepolymer får den til at bøje, som er grundlaget for sfærisk krystalvækst. Kredit:Drexel University Fra snef
- Hvem opdagede elektronmikroskoper?
- Sporing af floden:Mississippi-model kan hjælpe med at redde kysten
- Forskere bruger isotoper til at afsløre, hvordan akvifer genopfyldte 400, 000 år siden
- Smeltende is og en udgravning i høj højde afslører vikingehemmeligheder i Norge
- Hvorfor har planeter forskellige dag lenghts?
- Kæmpe radioteleskop vender sig mod en nyfundet planet i nærheden


