Hvad er Lewis -strukturen i CL2O7?
1. Beregn det samlede antal valenselektroner:
* Chlor (CL) har 7 valenselektroner, og der er to CL -atomer:7 * 2 =14 elektroner
* Oxygen (O) har 6 valenselektroner, og der er syv O -atomer:6 * 7 =42 elektroner
* Samlede valenselektroner:14 + 42 =56 elektroner
2. Bestem det centrale atom:
* Oxygen er mere elektronegativ end klor, så det vil være det centrale atom.
3. Tilslut atomerne med enkeltbindinger:
* Arranger de syv iltatomer omkring det centrale iltatom.
* Hvert iltatom danner en enkelt binding med det centrale iltatom.
4. Distribuer de resterende elektroner som ensomme par:
* Hvert iltatom har brug for to ensomme par for at afslutte sin oktet.
* Det centrale iltatom har brug for to ensomme par for at afslutte sin oktet.
5. Kontroller for formelle gebyrer:
* Den formelle ladning af et atom beregnes som:(valenselektroner) - (ikke -bindende elektroner) - (1/2 * bindingselektroner)
* De formelle afgifter skal minimeres for at opnå en stabil struktur.
6. Overvej flere obligationer:
* For at minimere formelle afgifter er vi nødt til at tilføje dobbeltbindinger mellem nogle af iltatomerne og det centrale iltatom.
* Den endelige struktur vil have tre dobbeltbindinger, med de andre fire oxygener, der er enkeltbundet til det centrale ilt.
Den sidste Lewis -struktur af Cl₂o₇:
`` `
O
/ \
Cl o
/ \ / \
O o o
/ \ / \ / \
Cl o o o
`` `
Nøglepunkter:
* Hvert kloratom er forbundet til to iltatomer med en dobbeltbinding og en enkelt binding.
* Det centrale iltatom har tre dobbeltbindinger og to ensomme par.
* Alle atomer har en komplet oktet af elektroner.
Bemærk: Der er resonansstrukturer for cl₂o₇, hvor dobbeltbindingerne kan skifte rundt. Imidlertid er strukturen vist ovenfor den mest almindelige og stabile repræsentation.
 Varme artikler
Varme artikler
-
 Solceller med nye grænsefladerKredit:CC0 Public Domain Forskere fra NUST MISIS (Rusland) og Tor Vergata-universitetet i Rom fandt ud af, at en mikroskopisk mængde todimensionalt titankarbid kaldet MXene forbedrer væsentligt op
Solceller med nye grænsefladerKredit:CC0 Public Domain Forskere fra NUST MISIS (Rusland) og Tor Vergata-universitetet i Rom fandt ud af, at en mikroskopisk mængde todimensionalt titankarbid kaldet MXene forbedrer væsentligt op -
 At skabe nul-energihuse, giftfri glitter og fossilfri lim med træNulenergihus Luukku. Kredit:Montse Zamorano At bygge klogt med træ er en effektiv måde at bekæmpe klimaændringer på. Det er muligt at bygge næsten alt med træ, hvis vi udvikler vores ekspertise og
At skabe nul-energihuse, giftfri glitter og fossilfri lim med træNulenergihus Luukku. Kredit:Montse Zamorano At bygge klogt med træ er en effektiv måde at bekæmpe klimaændringer på. Det er muligt at bygge næsten alt med træ, hvis vi udvikler vores ekspertise og -
 Forskere udvikler ny teknologi til udvinding af ikke-jernholdige og ædle metallerKredit:Ural Federal University Forskere ved Ruslands Ural Federal University (UrFU) arbejder på at løse problemet med at udvinde ikke-jernholdige og ædle metaller, som findes i malme, der er svære
Forskere udvikler ny teknologi til udvinding af ikke-jernholdige og ædle metallerKredit:Ural Federal University Forskere ved Ruslands Ural Federal University (UrFU) arbejder på at løse problemet med at udvinde ikke-jernholdige og ædle metaller, som findes i malme, der er svære -
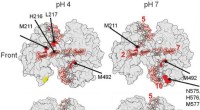 Undersøgelse afslører, hvordan iltfattigt protein binder løst til et mineralud på disse 3-D strukturelle gengivelser af proteinet, hjulpet forskere med at identificere, hvor proteinet binder til et mineral. De røde områder angiver mulige bindingsområder. Kredit:Berkeley Lab
Undersøgelse afslører, hvordan iltfattigt protein binder løst til et mineralud på disse 3-D strukturelle gengivelser af proteinet, hjulpet forskere med at identificere, hvor proteinet binder til et mineral. De røde områder angiver mulige bindingsområder. Kredit:Berkeley Lab
- Facebooks Zuckerberg er i fokus for den seneste behandlede video
- Silicium nanohole solceller har til formål at gøre solceller omkostningskonkurrencedygtige
- Hvad er meningen med dermal ostia i zoologi?
- Hård kærlighed til Amazons Bezos i Indien
- NASA forsvarer skrotning af alle kvinders rumvandring
- EPA-forslag vil ændre standarderne for sodforurening for første gang i 10 år:Hvad vi ved


