Hvad er 2s 2p i atom?
* 2 :Dette nummer angiver hovedkvantetal (n) , der definerer energiniveauet. Så 2 repræsenterer det andet energiniveau.
* s :Dette brev repræsenterer subshell , som er en specifik region inden for energiniveauet, hvor elektroner kan findes. "S" står for s subshell , som har en sfærisk form og kan indeholde maksimalt 2 elektroner .
* 2p :Dette repræsenterer p underskal , som er håndvægtformet og kan indeholde maksimalt 6 elektroner .
Derfor betyder "2S 2P", at der er 2 elektroner i underskalet på 2S og 2 i 2p underskalet For i alt 4 elektroner I det andet energiniveau.
Her er et eksempel:
* carbon (c) har et atomnummer på 6, hvilket betyder, at det har 6 elektroner. Dens elektronkonfiguration er 1S² 2s² 2p². Dette betyder, at 2 elektroner besætter underskalet på 2S, og 2 elektroner besætter underskalet 2P.
Vigtig note: Den faktiske fordeling af elektroner inden for 2p -underskalet kan variere afhængigt af atomet. Dette forklares af Hunds regel og Aufbau -princippet, men det overordnede koncept af "2s 2p" forbliver det samme.
 Varme artikler
Varme artikler
-
 Ved at tilføje belastning, forskere forbedrer metallisk glasFig. 1:Eksperimentel realisering af exciteret væskekøling. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00127-0 Metalliske glas - materialer med metalstyrke, men formbare som p
Ved at tilføje belastning, forskere forbedrer metallisk glasFig. 1:Eksperimentel realisering af exciteret væskekøling. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00127-0 Metalliske glas - materialer med metalstyrke, men formbare som p -
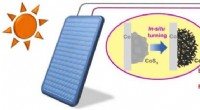 Ny elektrokatalysator udviklet til biomasseopgradering og brintgenereringDen fotovoltaiske elektrokatalyse til biomasseopgradering og brintgenerering. Kredit:NIMTE Prof. Zhang Jians team ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kine
Ny elektrokatalysator udviklet til biomasseopgradering og brintgenereringDen fotovoltaiske elektrokatalyse til biomasseopgradering og brintgenerering. Kredit:NIMTE Prof. Zhang Jians team ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kine -
 Prions:Nyt muligt terapeutisk mål opdagetprioner. Kredit:National Institute of Health Prionsygdomme, såsom bovin spongiform encephalopati (kogalskab), er dødelige neurodegenerative infektionssygdomme, som påvirker mennesker og andre patte
Prions:Nyt muligt terapeutisk mål opdagetprioner. Kredit:National Institute of Health Prionsygdomme, såsom bovin spongiform encephalopati (kogalskab), er dødelige neurodegenerative infektionssygdomme, som påvirker mennesker og andre patte -
 Skaber miljøvenlige lyddæmpere fra tangEn porøs film afledt af tang kunne være en mere bæredygtig lydabsorber end traditionelle skumpaneler. Kredit:ACS Sustainable Chemistry &Engineering Fra fly til lejligheder er de fleste rum nu desi
Skaber miljøvenlige lyddæmpere fra tangEn porøs film afledt af tang kunne være en mere bæredygtig lydabsorber end traditionelle skumpaneler. Kredit:ACS Sustainable Chemistry &Engineering Fra fly til lejligheder er de fleste rum nu desi
- Rumstrålingsdetektor kan hjælpe med at få øje på falske mesterværker
- University of Houston spin-off virksomhed rammer kommercielle milepæl
- Øre til jorden, lytter til atomsprængninger
- Hvor meget fisk spiser vi? Første globale fodaftryk for forbrug af fisk og skaldyr offentliggjort
- Hjælper immigranter og immigration økonomien?
- Hvordan ERF1 regulerer blomstringen


