Hvad er elektronkonfigurationen af MN i jordtilstand?
1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3d⁵
Her er en sammenbrud:
* 1S²: Det første energiniveau (n =1) har 2 elektroner i S -orbitalen.
* 2s² 2p⁶: Det andet energiniveau (n =2) har 2 elektroner i S -orbitalen og 6 elektroner i P -orbitalen.
* 3s² 3p⁶: Det tredje energiniveau (n =3) har 2 elektroner i S -orbitalen og 6 elektroner i P -orbitalen.
* 4S² 3d⁵: Det fjerde energiniveau (n =4) har 2 elektroner i S -orbitalen, og 3D -orbitalen har 5 elektroner.
Vigtig note: Du kan se elektronkonfigurationen skrevet som [AR] 4S² 3d⁵ også. Dette er en kortfattet notation ved hjælp af den ædle gas argon ([AR]) til at repræsentere de fyldte skaller op til 3p orbital.
 Varme artikler
Varme artikler
-
 Forskere offentliggør en komplet oversigt over sulfonimiddendrimererKredit:Skolkovo Institut for Videnskab og Teknologi Et forskerhold fra Skoltech Center for Design, Manufacturing and Materials (CDMM) har udarbejdet en omfattende oversigt over forskning i en fami
Forskere offentliggør en komplet oversigt over sulfonimiddendrimererKredit:Skolkovo Institut for Videnskab og Teknologi Et forskerhold fra Skoltech Center for Design, Manufacturing and Materials (CDMM) har udarbejdet en omfattende oversigt over forskning i en fami -
 Stigning af mandlige individer i stingless bier kolonier fører til dronninger dødUndersøgelse tyder på fremkomsten af hanbier med både faderligt og moderligt genetisk materiale ubalancer arbejdsstyrke i kolonier af Scaptotrigona depilis (fysogastrisk dronning inspicerer yngelc
Stigning af mandlige individer i stingless bier kolonier fører til dronninger dødUndersøgelse tyder på fremkomsten af hanbier med både faderligt og moderligt genetisk materiale ubalancer arbejdsstyrke i kolonier af Scaptotrigona depilis (fysogastrisk dronning inspicerer yngelc -
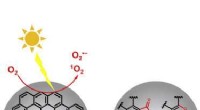 Partikelfasekemi gør det muligt for sod at spire skyer bedreMeget oxygenerede organiske molekyler med høj umættethed (HU-HOMer) dannes ved multigenerationel fotooxidation af store polycykliske aromatiske kulbrinter (PAHer) på sod. Kredit:Chem Meget oxygene
Partikelfasekemi gør det muligt for sod at spire skyer bedreMeget oxygenerede organiske molekyler med høj umættethed (HU-HOMer) dannes ved multigenerationel fotooxidation af store polycykliske aromatiske kulbrinter (PAHer) på sod. Kredit:Chem Meget oxygene -
 Kan atomkraft bekæmpe klimaændringer?Kredit:CC0 Public Domain For at afbøde klimaændringer, andelen af lavemissionselektricitetsproduktion skal stige fra nutidens 36 % til 85 % i 2040, siger det internationale energiagentur (IEA).
Kan atomkraft bekæmpe klimaændringer?Kredit:CC0 Public Domain For at afbøde klimaændringer, andelen af lavemissionselektricitetsproduktion skal stige fra nutidens 36 % til 85 % i 2040, siger det internationale energiagentur (IEA).
- Hvordan kan du bestemme, hvornår noget er tungere end den anden i rummet?
- Undersøgelse afslører, hvordan bakterielt patogen tilpasser sig ernæringsmæssig stress
- Hvorfor de rige i Jakarta har bedre adgang til vand end de fattige - det er ikke rørledningsnettet
- Sådan forklarer du fraktioner Trin for trin
- Ingen smerte, ingen gevinst? Konkret tænkning øger forbrugernes tillid
- Team forbedrer strukturel sundhedsovervågning med magnetostriktiv transducer


