Er fluor mere reaktiv end acylchlorid?
fluor betragtes som mere reaktiv end acylchlorider.
Her er hvorfor:
* fluorens høje elektronegativitet: Fluor er det mest elektronegative element, hvilket betyder, at det stærkt tiltrækker elektroner. Dette gør F-F-bindingen meget svag og tilbøjelig til at bryde, hvilket fører til stærkt reaktive fluoratomer.
* acylchlorides reaktivitet: Acylchlorider er reaktive på grund af den polariserede carbonylgruppe og den gode forladelsesgruppe (chlorid). De gennemgår let nukleofile acylsubstitutionsreaktioner.
Der er dog scenarier, hvor acylchlorider kan være mere reaktive:
* specifikke reaktionsbetingelser: Tilstedeværelsen af stærke baser eller nukleofiler kan aktivere acylchlorider og gøre dem mere reaktive end fluor i visse reaktioner.
* specifikke reaktanter: I reaktioner med specifikke reaktanter kan acylchlorider muligvis udvise højere reaktivitet på grund af faktorer som sterisk hindring eller elektroniske effekter.
Kortfattet: Mens fluor generelt betragtes som mere reaktiv på grund af dets høje elektronegativitet og svage binding, kan acylchlorider være mere reaktive under specifikke betingelser eller med specifikke reaktanter.
 Varme artikler
Varme artikler
-
 Maskinlæringsassisteret molekylært design til højtydende organiske fotovoltaiske materialerBrug af maskinlæring til at hjælpe molekylært design. Kredit:Wenbo Sun, Videnskabens fremskridt, doi:10.1126/sciadv.aay4275 At syntetisere højtydende materialer til organisk fotovoltaik (OPVer), d
Maskinlæringsassisteret molekylært design til højtydende organiske fotovoltaiske materialerBrug af maskinlæring til at hjælpe molekylært design. Kredit:Wenbo Sun, Videnskabens fremskridt, doi:10.1126/sciadv.aay4275 At syntetisere højtydende materialer til organisk fotovoltaik (OPVer), d -
 Ny tilgang forbedrer evnen til at forudsige metals reaktioner med vandVanddråbe. Billede:Wikimedia Commons Den brede rækkevidde af korrosion, et globalt problem på flere milliarder dollars, kan en dag blive indsnævret betydeligt takket være en ny, bedre tilgang til
Ny tilgang forbedrer evnen til at forudsige metals reaktioner med vandVanddråbe. Billede:Wikimedia Commons Den brede rækkevidde af korrosion, et globalt problem på flere milliarder dollars, kan en dag blive indsnævret betydeligt takket være en ny, bedre tilgang til -
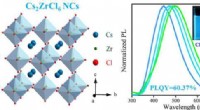 Forskere syntetiserer blyfrit zirkoniumbaseret ledigt bestilt dobbelt perovskit-nanokrystallerBlyfri perovskit Cs2ZrCl6 NCer med en PLQY op til 60,37% syntetiseres. Kredit:LIU Siping og YANG Bin I de seneste år, uorganisk CsPbX 3 (X =Cl, Br, I) peranovskite -nanokrystaller har tiltrukket
Forskere syntetiserer blyfrit zirkoniumbaseret ledigt bestilt dobbelt perovskit-nanokrystallerBlyfri perovskit Cs2ZrCl6 NCer med en PLQY op til 60,37% syntetiseres. Kredit:LIU Siping og YANG Bin I de seneste år, uorganisk CsPbX 3 (X =Cl, Br, I) peranovskite -nanokrystaller har tiltrukket -
 Kunstig fotosynteseteknologi dukker opKulstofunderstøttet wolframfrøbaseret 3D-sølv-dendritkatalysator. Kredit:Korea Institute of Science and Technology (KIST) Koreanske forskere bestræber sig på at gøre kunstig fotosynteseteknologi t
Kunstig fotosynteseteknologi dukker opKulstofunderstøttet wolframfrøbaseret 3D-sølv-dendritkatalysator. Kredit:Korea Institute of Science and Technology (KIST) Koreanske forskere bestræber sig på at gøre kunstig fotosynteseteknologi t
- Hvad er asteroider lavet af?
- Apollo-eksperimentet, der bliver ved med at give
- Hvorfor ser vi månen?
- Forskere måler med succes nogle af elektronernes kvanteegenskaber i 2-D halvledere
- Nethindescanninger og fingeraftrykstjek:højteknologisk eller høj risiko?
- Glem smarte byer (i et minut), vi skal tale om smarte gårde


