Hvad ville der ske med pres, når mængden af gas blev halveret?
Dette betyder, at hvis du halverer mængden af en gas , presset vil dobbelt .
Her er en simpel forklaring:
* Forestil dig en fast mængde gasmolekyler i en beholder.
* Når du reducerer volumen (gør beholderen mindre), har gasmolekylerne mindre plads til at bevæge sig rundt.
* Dette betyder, at de kolliderer med containerens vægge oftere.
* Flere kollisioner betyder mere kraft, der udøves på væggene, hvilket resulterer i højere pres.
Formel:
Boyle's lov kan udtrykkes matematisk som:
P₁v₁ =p₂v₂
Hvor:
* P₁ =oprindeligt tryk
* V₁ =indledende bind
* P₂ =endelig pres
* V₂ =slutvolumen
I dit scenarie, hvis V₂ =V₁/2, så p₂ =2p₁.
 Varme artikler
Varme artikler
-
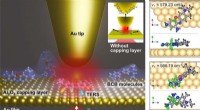 Iagttagelse af forskellen i strukturel dynamik af 1 nm enkeltmolekyler ved stuetemperatur for først…(Venstre) Illustration af isolerede molekyler fanget mellem guld- og aluminiumoxidlag ved hjælp af en spidsforstærket nanoskopi. (Højre) Visualisering af vibrationstilstandene for et brillant cresylbl
Iagttagelse af forskellen i strukturel dynamik af 1 nm enkeltmolekyler ved stuetemperatur for først…(Venstre) Illustration af isolerede molekyler fanget mellem guld- og aluminiumoxidlag ved hjælp af en spidsforstærket nanoskopi. (Højre) Visualisering af vibrationstilstandene for et brillant cresylbl -
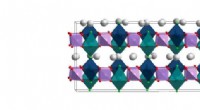 Ny genomisk metode afslører atomarrangementer af batterimaterialeLavtemperaturstrukturen af NVPF [Na3V2(PO4)2F3] løst i dette arbejde. Beregninger fra Lawrence Berkeley National Laboratory tyder på, at natriumatomerne (hvide) lettest kan bevæge sig i flyene melle
Ny genomisk metode afslører atomarrangementer af batterimaterialeLavtemperaturstrukturen af NVPF [Na3V2(PO4)2F3] løst i dette arbejde. Beregninger fra Lawrence Berkeley National Laboratory tyder på, at natriumatomerne (hvide) lettest kan bevæge sig i flyene melle -
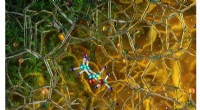 Neutroner optimerer højeffektiv katalysator for en grønnere tilgang til biobrændstofsynteseIllustration af den optimerede zeolitkatalysator (NbAlS-1), som muliggør en højeffektiv kemisk reaktion for at skabe buten, en vedvarende energikilde, uden at bruge store mængder energi til konverteri
Neutroner optimerer højeffektiv katalysator for en grønnere tilgang til biobrændstofsynteseIllustration af den optimerede zeolitkatalysator (NbAlS-1), som muliggør en højeffektiv kemisk reaktion for at skabe buten, en vedvarende energikilde, uden at bruge store mængder energi til konverteri -
 Origami inspirerer til ny teknologi til vævsregenereringUMass Lowell Prof. Gulden Camci-Unal arbejder sammen med studerende Xinchen Wu om biomaterialeforskning ved universitetets Saab Emerging Technologies and Innovation Center. Kredit:Edwin Aguirre for UM
Origami inspirerer til ny teknologi til vævsregenereringUMass Lowell Prof. Gulden Camci-Unal arbejder sammen med studerende Xinchen Wu om biomaterialeforskning ved universitetets Saab Emerging Technologies and Innovation Center. Kredit:Edwin Aguirre for UM


