Hvad er Q -værdi i opløsning?
Her er en sammenbrud:
* q er produktet af koncentrationerne af ionerne i opløsning hævet til deres respektive støkiometriske koefficienter i den afbalancerede opløsningsreaktion. For eksempel til opløsning af sølvchlorid (AGCL):
`` `
AGCL (s) <=> AG + (aq) + Cl- (aq)
`` `
Q-værdien beregnes som:Q =[AG+] [cl-].
* Q -værdi kan bruges til at forudsige retningen for opløsningsprocessen:
* q
* q> ksp: Opløsningen er overmættet, hvilket betyder, at det faste stof udfældes.
* q =ksp: Opløsningen er mættet, hvilket betyder, at opløsningshastigheden og nedbør er ens.
* KSP er opløselighedsproduktet , en konstant, der repræsenterer den maksimale mængde af ioner, der kan opløses i en opløsning ved en given temperatur.
I det væsentlige giver Q et øjebliksbillede af de relative mængder af ioner i opløsning på et givet tidspunkt og kan bruges til at forstå retningen for opløsningsprocessen i forhold til ligevægt.
Her er nogle yderligere punkter:
* Q -værdien ligner reaktionskvotienten (Q), der bruges i kemisk kinetik, men den anvendes specifikt til opløsningsreaktioner.
* Q -værdi er et nyttigt værktøj til at forudsige opløseligheden af salte og andre ioniske forbindelser.
Fortæl mig, hvis du har andre spørgsmål.
Sidste artikelHvad er substantivformen med at opløse?
Næste artikelEr pH 4 stærkere end PH3?
 Varme artikler
Varme artikler
-
 Skræddersyede materialer med ultrahurtige forbindelserNår atomisk tynde lag af to materialer stables og snoes, et heterostruktur-materiale opstår. En ny forbindelse er dannet, næsten øjeblikkeligt, med specielle energitilstande - kendt som interlayer exc
Skræddersyede materialer med ultrahurtige forbindelserNår atomisk tynde lag af to materialer stables og snoes, et heterostruktur-materiale opstår. En ny forbindelse er dannet, næsten øjeblikkeligt, med specielle energitilstande - kendt som interlayer exc -
 At belyse, hvordan asymmetri giver kemiske egenskaberKredit:CC0 Public Domain Du har hørt udtrykket form følger funktion? I materialevidenskab, funktion følger form. Ny forskning af Carnegies Olivier Gagné og samarbejdspartner Frank Hawthorne fra U
At belyse, hvordan asymmetri giver kemiske egenskaberKredit:CC0 Public Domain Du har hørt udtrykket form følger funktion? I materialevidenskab, funktion følger form. Ny forskning af Carnegies Olivier Gagné og samarbejdspartner Frank Hawthorne fra U -
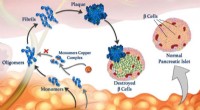 Kobberioner kan spille en nøglerolle, når peptidfoldning går galtKobberioner (røde kugler) kan vedhæfte peptidmonomerer (blå) og forhindre dem i at klumpe sig sammen for at danne oligomerer, fibriller og skadelige plaketter. © 2020 Mawadda Alghrably Afvikling a
Kobberioner kan spille en nøglerolle, når peptidfoldning går galtKobberioner (røde kugler) kan vedhæfte peptidmonomerer (blå) og forhindre dem i at klumpe sig sammen for at danne oligomerer, fibriller og skadelige plaketter. © 2020 Mawadda Alghrably Afvikling a -
 Forskere opretter den første milliard-atom biomolekylære simuleringEt Los Alamos-ledet team skabte den hidtil største simulering af et helt DNA-gen, en bedrift, der krævede en milliard atomer for at modellere. Kredit:Los Alamos National Laboratory Forskere ved Lo
Forskere opretter den første milliard-atom biomolekylære simuleringEt Los Alamos-ledet team skabte den hidtil største simulering af et helt DNA-gen, en bedrift, der krævede en milliard atomer for at modellere. Kredit:Los Alamos National Laboratory Forskere ved Lo
- $500 milliarder spørgsmål:Hvad er værdien af at studere havets biologiske kulstofpumpe?
- Hvad er en karyotype?
- Hvad er energiomdannelsen i en hånddrevet generator?
- Hvad mener du med brændstofværdi af brændstoffer, og hvordan kan det bestemme den farvevæskede f…
- Gennembrud i at forudsige kaotiske udfald i tre-kropssystemer
- Udløste ekstreme udsving i ilt, ikke en gradvis stigning, den kambriske eksplosion?


