Opløses en kold eller varm væske hurtigere gas hurtigere?
Forklaring:
* opløselighed af gasser: Gasser er mere opløselige i væsker ved lavere temperaturer. Dette skyldes, at gasmolekylerne har mindre kinetisk energi og er mindre tilbøjelige til at flygte fra væsken.
* kinetisk energi og temperatur: Når temperaturen på en væske øges, øges de kinetiske energi af væskemolekylerne også. Denne øgede kinetiske energi får væskemolekylerne til at bevæge sig hurtigere og kollidere med gasmolekylerne hyppigere.
* Gas Escape: De øgede kollisioner mellem væske- og gasmolekylerne gør det lettere for gasmolekylerne at flygte fra væsken, hvilket reducerer gasens opløselighed.
Kortfattet:
* kolde væsker: Nedre kinetisk energi, mindre gasudslip, højere opløselighed.
* varme væsker: Højere kinetisk energi, mere gasudslip, lavere opløselighed.
Eksempel:
* En kulsyreholdig drik vil gå fladt hurtigere ved stuetemperatur end i køleskabet, fordi kuldioxidgassen er mere opløselig i den kolde drik.
Derfor opløses en varm væske hurtigere, fordi den højere temperatur får gasmolekylerne til at undslippe lettere.
Sidste artikelHvad hedder varm gas?
Næste artikelHvad er egenskaberne ved fast væske og gas?
 Varme artikler
Varme artikler
-
 Ny sensor kan snart teste for coronavirus og influenza samtidigtDenne sensor er på størrelse med et mikro-USB-drev og er i stand til at teste for influenza og COVID-19 samtidigt. Kredit:Dmitry Kireev, University of Texas i Austin Den nye coronavirus er blevet
Ny sensor kan snart teste for coronavirus og influenza samtidigtDenne sensor er på størrelse med et mikro-USB-drev og er i stand til at teste for influenza og COVID-19 samtidigt. Kredit:Dmitry Kireev, University of Texas i Austin Den nye coronavirus er blevet -
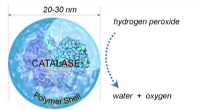 Fælles antioxidantenzym kan give potentiel behandling for COVID-19Simpelt diagram, der viser katalase kickstartreaktion, der omdanner hydrogenperoxid til vand og oxygen. Kredit:Yunfeng Lu forskningsgruppe/UCLA Forskere fra UCLA og Kina har fundet ud af, at katal
Fælles antioxidantenzym kan give potentiel behandling for COVID-19Simpelt diagram, der viser katalase kickstartreaktion, der omdanner hydrogenperoxid til vand og oxygen. Kredit:Yunfeng Lu forskningsgruppe/UCLA Forskere fra UCLA og Kina har fundet ud af, at katal -
 Varmebehandling giver præcis kontrol over katalytisk aktivitet af metalsulfidnanopartiklerDette scanningselektronmikroskopbillede (forstørrelse x100, 000) viser overfladen af et porøst nikkelskum, der er krydret med katalytiske nanopartikler af koboltsulfid og nikkelsulfid. Kredit:A*STAR
Varmebehandling giver præcis kontrol over katalytisk aktivitet af metalsulfidnanopartiklerDette scanningselektronmikroskopbillede (forstørrelse x100, 000) viser overfladen af et porøst nikkelskum, der er krydret med katalytiske nanopartikler af koboltsulfid og nikkelsulfid. Kredit:A*STAR -
 Gaslagringsmetode kan hjælpe næste generation af ren energikøretøjerMeget porøs programmerbar svamp til opbevaring af ren energi. Kredit:Northwestern University Et forskerhold ledet af Northwestern University har designet og syntetiseret nye materialer med ultrahø
Gaslagringsmetode kan hjælpe næste generation af ren energikøretøjerMeget porøs programmerbar svamp til opbevaring af ren energi. Kredit:Northwestern University Et forskerhold ledet af Northwestern University har designet og syntetiseret nye materialer med ultrahø
- Kan du bruge sølvsulfadiazin på Poison Ivy?
- Registrering og identifikation af sprængstof med en enkelt test
- Hvor mange trin i en kilometer?
- Metamorfose er nødvendig i iværksætteri og ledelse, siger banebrydende økonom
- Forskere løfter sløret for elektronik, der efterligner den menneskelige hjerne i effektiv læring
- Hvordan sindets grænser former det menneskelige sprog


