Hvad er det samlede antal valenselektroner i IBR?
* Valenselektroner: Valenselektroner er elektronerne i den yderste skal af et atom. Det er dem, der er involveret i kemisk binding.
* gruppenumre: Gruppenummeret for et element i den periodiske tabel fortæller dig, hvor mange valenselektroner det har (for hovedgruppelementer).
1. jod (i): Jod er i gruppe 17 (også kendt som gruppe VIIA), så det har 7 valenselektroner.
2. brom (Br): Brom er også i gruppe 17, så den har 7 valenselektroner.
3. Samlede valenselektroner: 7 (fra jod) + 7 (fra brom) = 14 valenselektroner
Derfor er der i alt 14 valenselektroner i IBR -molekylet.
Sidste artikelHvor mange bindings- og ikke-bindende elektronpar findes i BF3-molekylerne?
Næste artikelEr brintgas og ammoniak eksplosiv?
 Varme artikler
Varme artikler
-
 Video:Hvad skete der præcist i Tjernobyl?Kredit:The American Chemical Society Den 26. april, 1986, Sovjetunionens atomreaktor 4 i Tjernobyl Power Complex eksploderede. Denne uge om reaktioner, vi taler om kemien bag denne katastrofale b
Video:Hvad skete der præcist i Tjernobyl?Kredit:The American Chemical Society Den 26. april, 1986, Sovjetunionens atomreaktor 4 i Tjernobyl Power Complex eksploderede. Denne uge om reaktioner, vi taler om kemien bag denne katastrofale b -
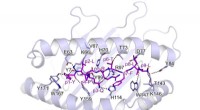 Afdækning af, hvordan T-celler genkender SARS-COV-2 virus spike proteinStruktur af HLA-A2S269-277. H-bindingsinteraktioner mellem S269-277-peptidet (lilla pinde) og HLA-A2 (tegneserie). HLA-A2-kontaktrester og H-bindinger inden for 3,5 Å af peptidet er vist (lyseblå pind
Afdækning af, hvordan T-celler genkender SARS-COV-2 virus spike proteinStruktur af HLA-A2S269-277. H-bindingsinteraktioner mellem S269-277-peptidet (lilla pinde) og HLA-A2 (tegneserie). HLA-A2-kontaktrester og H-bindinger inden for 3,5 Å af peptidet er vist (lyseblå pind -
 Trænger undervisning og kommunikation om mikrofluidiske fremskridt til forbedring?I Biomikrofluidik , forskere præsenterer en gennemgang af publiceret litteratur om mikrofluidikundervisning og giver metoder og forslag til forbedring af mikrofluidiklære og -opsøgende. Dette billed
Trænger undervisning og kommunikation om mikrofluidiske fremskridt til forbedring?I Biomikrofluidik , forskere præsenterer en gennemgang af publiceret litteratur om mikrofluidikundervisning og giver metoder og forslag til forbedring af mikrofluidiklære og -opsøgende. Dette billed -
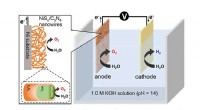 Et skridt nærmere en brintdrevet økonomi ved hjælp af en effektiv anode til vandopdelingSkematisk repræsentation af vanddissociationsprocessen ved lavt overpotentiale på ca. 32 mV ved anvendelse af NiS x nanotråde proppet ind i C 3 N 4 skede som anode til vandoxidation. Kredit:Niig
Et skridt nærmere en brintdrevet økonomi ved hjælp af en effektiv anode til vandopdelingSkematisk repræsentation af vanddissociationsprocessen ved lavt overpotentiale på ca. 32 mV ved anvendelse af NiS x nanotråde proppet ind i C 3 N 4 skede som anode til vandoxidation. Kredit:Niig
- Hvilken slags videnskabsmand er involveret i forskning relateret til biologiske systemer og menneske…
- Hvorfor du burde have mere sympati for måger, og hvordan du forhindrer dem i at stjæle dine chips
- Hvad er processer inden for videnskab eller videnskabelige processer?
- Hvilken slags barometer måler lufttrykket ved at bruge et metalkammer, der er følsomt over for æn…
- X-ray satellit XMM-Newton fejrer 20 år i rummet
- Hvad er de seks menneskelige sanser?


