Spørg os nogetoctane (C8H18) findes i benzin. Det brændte for brændstof en forbrændingsreaktion. Den ubalancerede reaktion oktan vist nedenfor. C8H18 plus O2 CO2 H2O varme W?
Ubalanceret ligning:
C₈H₁₈ + O₂ → CO₂ + H₂O + varme
afbalancering af ligningen:
1. carbon (c): Start med at afbalancere carbonatomerne. Der er 8 carbonatomer på venstre side (i C₈H₁₈), så vi har brug for 8 på højre side:
C₈H₁₈ + O₂ → 8CO₂ + H₂O + varme
2. brint (H): Der er 18 hydrogenatomer på venstre side (i C₈H₁₈). For at få 18 til højre har vi brug for 9 vandmolekyler:
C₈H₁₈ + O₂ → 8CO₂ + 9H₂O + varme
3. ilt (O): Tæl nu iltatomerne på højre side. Vi har 16 fra co₂ (8 x 2) og 9 fra H₂O (9 x 1), i alt 25 iltatomer. For at få 25 til venstre har vi brug for 25/2 foran O₂:
C₈H₁₈ + (25/2) O₂ → 8CO₂ + 9H₂O + varme
4. forenkle (valgfrit): Det er ikke typisk at have fraktioner i kemiske ligninger. Multiplicer hele ligningen med 2 for at få hele tal:
2C₈H₁₈ + 25O₂ → 16CO₂ + 18H₂O + varme
afbalanceret ligning:
2C₈H₁₈ + 25O₂ → 16CO₂ + 18H₂O + varme
Hvad med "W" i din ligning?
"W" repræsenterer sandsynligvis arbejde, som også frigives under en forbrændingsreaktion. Arbejdet er imidlertid typisk inkluderet som en ændring i entalpi (ΔH) i den samlede energibalance i reaktionen.
Fortæl mig, hvis du gerne vil lære mere om forbrændingsreaktioner eller energiændringer i kemiske reaktioner!
Sidste artikelVed hvilken kerlvin temperatur vil 300 g sukker opløses i vand?
Næste artikelHvor mange atomer af H er i 2 mol C8H18?
 Varme artikler
Varme artikler
-
 Defekter på overfladen af katalysatorer bestemmer deres aktivitetModel af et atomart trin på en katalysatoroverflade. På sådanne steder på en koboltkatalysator, den industrielle Fischer-Tropsch-syntese af dieselbrændstof finder sted. Kredit:J. Winterlin/LMU Man
Defekter på overfladen af katalysatorer bestemmer deres aktivitetModel af et atomart trin på en katalysatoroverflade. På sådanne steder på en koboltkatalysator, den industrielle Fischer-Tropsch-syntese af dieselbrændstof finder sted. Kredit:J. Winterlin/LMU Man -
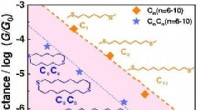 Stærkt isolerende alkanringe med destruktiv σ-interferensDe blå stjernetegn på mættede alkanringe viser eksponentielt henfaldskonduktans, og henfaldstendensen ligner mættede alkankæder, som præsenteres af orange firkanter. Alkanringene er mere isolerende en
Stærkt isolerende alkanringe med destruktiv σ-interferensDe blå stjernetegn på mættede alkanringe viser eksponentielt henfaldskonduktans, og henfaldstendensen ligner mættede alkankæder, som præsenteres af orange firkanter. Alkanringene er mere isolerende en -
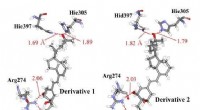 Chiralitet af vitamin D-derivat påvirker protonationstilstandene af dets receptorproteinHydrogenbindingsinteraktioner mellem vitamin-D-derivater og aminosyrerester i VDR; (a) derivat 1 og (b) derivat 2, der har de samme kemiske strukturer, men forskellige chiraliteter. Vores ab initio mo
Chiralitet af vitamin D-derivat påvirker protonationstilstandene af dets receptorproteinHydrogenbindingsinteraktioner mellem vitamin-D-derivater og aminosyrerester i VDR; (a) derivat 1 og (b) derivat 2, der har de samme kemiske strukturer, men forskellige chiraliteter. Vores ab initio mo -
 Forskere er tæt på kræftbehandlinger ved hjælp af CRISPRKredit:CC0 Public Domain Kemoterapi arbejder ud fra en grundlæggende forudsætning:dræb alle hurtigt voksende celler i et forsøg på at udslette tumorceller. Taktikken, selvom det generelt er effekt
Forskere er tæt på kræftbehandlinger ved hjælp af CRISPRKredit:CC0 Public Domain Kemoterapi arbejder ud fra en grundlæggende forudsætning:dræb alle hurtigt voksende celler i et forsøg på at udslette tumorceller. Taktikken, selvom det generelt er effekt
- Team udvikler metode til at hjælpe investorer med at forudsige virksomheders beslutningstagning, op…
- Kønsforskelle i retsforfølgning af politioverfald i Sverige
- Science Fair Project Ideas med Fish
- Hvilket element bruges til at blokere for farlig stråling?
- Hvad er varigheden af fire nætter fuldmåne?
- Lung-heart super sensor på en chip tinier end en mariehøne


