Hvor mange elektroner mister overgangsmetaller?
* Variabel oxidation siger: Overgangsmetaller er kendt for at have flere oxidationstilstande. Dette betyder, at de kan miste et varierende antal elektroner afhængigt af det kemiske miljø, de er i.
* Elektronkonfiguration: Deres elektronkonfiguration involverer delvist fyldte D-orbitaler, som giver dem mulighed for let at miste elektroner fra både deres S og D-orbitaler.
* Eksempler:
* Jern (Fe) kan have oxidationstilstande på +2 (mister 2 elektroner) eller +3 (mister 3 elektroner).
* Kobber (Cu) kan have oxidationstilstande på +1 (mister 1 elektron) eller +2 (mister 2 elektroner).
Generelle tendenser:
* gruppe 3-7: Disse metaller mister typisk elektroner fra deres 4s orbital først og derefter fra deres 3D -orbital.
* gruppe 8-10: Disse metaller har en tendens til at miste elektroner fra både deres 4'ere og 3D -orbitaler samtidigt.
* gruppe 11-12: Disse metaller mister primært elektroner fra deres 4s orbital.
Det er vigtigt at huske, at antallet af elektroner, en overgangsmetal mister, afhænger af den specifikke kemiske reaktion og den resulterende forbindelse.
Sidste artikelHvad er det kemiske symbol på ethanol og vand?
Næste artikelHvad står den kemiske formel nuco2 for?
 Varme artikler
Varme artikler
-
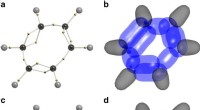 Efter 90 år, forskere afslører strukturen af benzenDVMS -strukturer til benzen. et Voronoi-sted til RHF/6-31G (d) bølgefunktion. Elektronpositionerne for et vilkårligt spin vises som små gule kugler. b Tværsnit gennem bølgefunktionen omkring Voronoi -
Efter 90 år, forskere afslører strukturen af benzenDVMS -strukturer til benzen. et Voronoi-sted til RHF/6-31G (d) bølgefunktion. Elektronpositionerne for et vilkårligt spin vises som små gule kugler. b Tværsnit gennem bølgefunktionen omkring Voronoi - -
 Enkeltcelleanalyse afslører heterogenitet i metaladsorptionKredit:LuckyStep/Shutterstock Biosorption er fjernelse af kontaminanter fra en prøve ved at adsorbere dem på overfladen af et biologisk materiale. Det forventes at give miljømæssige og økonomiske
Enkeltcelleanalyse afslører heterogenitet i metaladsorptionKredit:LuckyStep/Shutterstock Biosorption er fjernelse af kontaminanter fra en prøve ved at adsorbere dem på overfladen af et biologisk materiale. Det forventes at give miljømæssige og økonomiske -
 Ny proces kan forlænge metallernes levetidKredit:Skylar Kang fra Pexels Stærkere, lettere, billigere materialer er navnet på spillet i avanceret fremstilling. At holde omkostningerne nede på materialer, der er ens, hvis ikke mere, effekti
Ny proces kan forlænge metallernes levetidKredit:Skylar Kang fra Pexels Stærkere, lettere, billigere materialer er navnet på spillet i avanceret fremstilling. At holde omkostningerne nede på materialer, der er ens, hvis ikke mere, effekti -
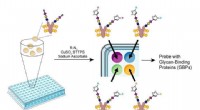 Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
- Hvad vil der ske med planter, hvis der ikke er nogen varmeenergi?
- Undersøgelse viser, at mediernes visuelle rammer i debatter påvirker offentlighedens opfattelse
- Hvad var resultaterne af hans første eksperiment?
- Hvad er 5 eksempler på enkel multiple transformationsenergi?
- Hvad sker der, når en lysstråle rettes mod spejlet?
- HBS -allel -seglcellen forekommer ved en højere frekvens i Afrika end det gør USA fordi?


