Hvad er elektronkonfigurationen for ilt og svovl?
ilt (O):
* Fuld konfiguration: 1S² 2S² 2P⁴
* kortfattet konfiguration: [Han] 2S² 2P⁴
svovl (er):
* Fuld konfiguration: 1S² 2S² 2P⁶ 3S² 3P⁴
* kortfattet konfiguration: [Ne] 3S² 3P⁴
Forklaring:
* Elektronkonfiguration: Beskriver arrangementet af elektroner i et atoms energiniveau og orbitaler.
* hovedkantenummer (n): Angiver energiniveauet (f.eks. 1, 2, 3).
* Sublevel (S, P, D, F): Angiver formen på orbitalen.
* s: Sfærisk
* p: Håndvægtformet
* D: Mere komplekse former
* f: Endnu mere komplekse former
* antal elektroner: Superscript angiver antallet af elektroner i det underniveau.
* kortfattet konfiguration: Bruger den forrige ædle gas til at forenkle konfigurationen.
Nøglepunkter:
* ilt og svovl er i den samme gruppe (gruppe 16 eller chalcogens). Dette betyder, at de har lignende valenselektronkonfigurationer, hvilket fører til lignende kemiske egenskaber.
* Valenselektroner: De yderste elektroner (i det højeste energiniveau) er ansvarlige for et elements reaktivitet. For både ilt og svovl er deres valenselektroner i P -sublet.
Fortæl mig, hvis du har andre spørgsmål om elektronkonfiguration!
 Varme artikler
Varme artikler
-
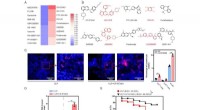 PDGFR-kinasehæmmer fundet at beskytte mod septisk død via regulering af BTLAA, Heatmap, der afbilder virkningen af lægemiddelbiblioteksinhibitorer på ekspressionsniveauet af BTLA i RAW264.7-celler ved in-celle western blotting. De 10 bedste lægemidler, der hæmmer (venstre)
PDGFR-kinasehæmmer fundet at beskytte mod septisk død via regulering af BTLAA, Heatmap, der afbilder virkningen af lægemiddelbiblioteksinhibitorer på ekspressionsniveauet af BTLA i RAW264.7-celler ved in-celle western blotting. De 10 bedste lægemidler, der hæmmer (venstre) -
 Reducerer smeltede salte ætsende virkningDette diagram viser, hvordan et koncentrerende solvarmeanlæg kunne bruge smeltede salte til at lagre solenergi, som senere kunne bruges til at generere elektricitet. Kredit:Jaimee Janiga/ORNL, U.S. De
Reducerer smeltede salte ætsende virkningDette diagram viser, hvordan et koncentrerende solvarmeanlæg kunne bruge smeltede salte til at lagre solenergi, som senere kunne bruges til at generere elektricitet. Kredit:Jaimee Janiga/ORNL, U.S. De -
 Kunstig intelligens møder materialevidenskabEt Texas A&M Engineering-forskerhold udnytter kraften ved maskinlæring og kunstig intelligens til at skabe en open source-softwarepakke, der selvstændigt opdager nye materialer. Kredit:Texas A&M Unive
Kunstig intelligens møder materialevidenskabEt Texas A&M Engineering-forskerhold udnytter kraften ved maskinlæring og kunstig intelligens til at skabe en open source-softwarepakke, der selvstændigt opdager nye materialer. Kredit:Texas A&M Unive -
 Forskere får kontrol over syntesen af bløde molekylerKemisk og biomolekylær ingeniørprofessor Damien Guironnet, ret, og kandidatstuderende Dylan Walsh udviklede en ny teknik, der giver dem mulighed for at programmere størrelsen, form og sammensætning af
Forskere får kontrol over syntesen af bløde molekylerKemisk og biomolekylær ingeniørprofessor Damien Guironnet, ret, og kandidatstuderende Dylan Walsh udviklede en ny teknik, der giver dem mulighed for at programmere størrelsen, form og sammensætning af
- Hvor forekommer reaktioner i en elektrolytisk celle?
- Universet er et hologram og andre tankevækkende teorier inden for teoretisk fysik
- Hvilken reaktant var den begrænsende i eddikelaboratoriet?
- Din pension har en stor rolle at spille i bekæmpelsen af klimaændringer – her er, hvordan du gø…
- Hvad går tabt, når solen smelter sammen med brint til helium?
- Nævn tre ikke-silikatmineraler, der almindeligvis findes i klipper?


