Hvilket stof dannes på en kobbermetaloverflade i sølvnitratopløsningen?
Her er sammenbruddet:
* kobber (cu) er mere reaktiv end sølv (AG) .
* I opløsningen findes sølvnitrat (Agno₃) som sølvioner (Ag⁺) og nitrationer (NO₃⁻).
* Kobberatomerne donerer elektroner til sølvionerne, hvilket får sølvionerne til at reducere og blive fast sølvmetal.
* Kobberatomerne oxideres og bliver kobberioner (Cu²⁺), som derefter opløses i opløsningen.
Den kemiske reaktion er:
cu (s) + 2agno₃ (aq) → 2ag (s) + cu (no₃) ₂ (aq)
Kortfattet: Stoffet dannet på kobbermetaloverfladen er fast sølvmetal (AG) .
Sidste artikelHvad er pH -niveauet for en meget sur opløsning?
Næste artikelHvad skal vanddamp blive til dråber?
 Varme artikler
Varme artikler
-
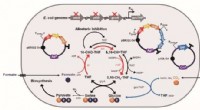 Konstrueret E. coli ved hjælp af myresyre og CO2 som en C1-raffinaderiplatformstammeMyresyre- og CO2-assimileringsveje bestående af den rekonstruerede THF-cyklus og omvendt glycin-spaltningsreaktion. Dette skematiske diagram viser myresyre- og CO2-assimileringsproceduren gennem vejen
Konstrueret E. coli ved hjælp af myresyre og CO2 som en C1-raffinaderiplatformstammeMyresyre- og CO2-assimileringsveje bestående af den rekonstruerede THF-cyklus og omvendt glycin-spaltningsreaktion. Dette skematiske diagram viser myresyre- og CO2-assimileringsproceduren gennem vejen -
 Justerbare omvendte fotokromer i fast tilstandKredit:ICN2 Fotokrome er farvestoffer, der ændrer deres farve afhængigt af det lys, de modtager. Når lyset er slukket, kan de enten forblive i deres fotoinducerede tilstand (P-type fotokromer) ell
Justerbare omvendte fotokromer i fast tilstandKredit:ICN2 Fotokrome er farvestoffer, der ændrer deres farve afhængigt af det lys, de modtager. Når lyset er slukket, kan de enten forblive i deres fotoinducerede tilstand (P-type fotokromer) ell -
 Smartphone-baseret enhed til detektering af norovirus, krydstogtskibsmikrobenEn følsom ny enhed kan registrere små mængder norovirus i vand. Kredit:American Chemical Society gjort berygtet af udbrud på krydstogtskibe, norovirus kan virkelig ødelægge en ferie, forårsager al
Smartphone-baseret enhed til detektering af norovirus, krydstogtskibsmikrobenEn følsom ny enhed kan registrere små mængder norovirus i vand. Kredit:American Chemical Society gjort berygtet af udbrud på krydstogtskibe, norovirus kan virkelig ødelægge en ferie, forårsager al -
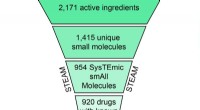 EN SKY af muligheder:At finde nye terapier ved at kombinere lægemidlerSkematisk repræsentation af filtrerings- og klyngeproceduren, der fører til 308 CLOUD-lægemidlerne. Kredit:(c) Naturens kemiske biologi / Stefan Kubicek CeMM Library of Unique Drugs (CLOUD) er d
EN SKY af muligheder:At finde nye terapier ved at kombinere lægemidlerSkematisk repræsentation af filtrerings- og klyngeproceduren, der fører til 308 CLOUD-lægemidlerne. Kredit:(c) Naturens kemiske biologi / Stefan Kubicek CeMM Library of Unique Drugs (CLOUD) er d
- Hvorfor forekommer solen lyseste blandt stjerner?
- Sne kan have forsinket nogle opblomstringer til den første dag i foråret
- Jordbundsundersøgelser giver spor til oldtidens klima
- Forskere har fundet en måde at skabe lægemiddelmolekyler ud fra kulilte
- Hvad er de tre tidsperioder, som dinosaurerne levede i?
- Hvordan vi opdagede den mærkelige fysik af jetfly fra supermassive sorte huller


