Hvilket trin er ikke en brugt til afbalancering af kemisk ligning?
Her er hvorfor:
* afbalancering af kemiske ligninger betyder at sikre, at antallet af atomer i hvert element på reaktantsiden (venstre side) af ligningen er lig med antallet af atomer i dette element på produktsiden (højre side).
* underskrifter I en kemisk formel angiver antallet af atomer af dette element i et molekyle. Ændring af et underskrift ville ændre identiteten af selve molekylet, hvilket ikke er tilladt, når man afbalancerer ligninger.
* Koefficienter er tallene placeret foran kemiske formler. Disse bruges til at justere antallet af molekyler af hvert stof i reaktionen, hvilket muliggør en afbalanceret ligning.
Her er et eksempel:
ubalanceret: H₂ + O₂ → H₂O
afbalanceret: 2H₂ + O₂ → 2H₂O
Vi tilføjede koefficienter (2 foran H₂ og 2 foran H₂O) for at afbalancere ligningen. Vi gjorde ikke Skift underskrifterne inden for formlerne (som at ændre H₂O til H₂O₂).
 Varme artikler
Varme artikler
-
 Fra drivhusgasser til plast:Ny katalysator til genanvendelse af kuldioxid opdagetOverfladen på en nanostruktureret kobberkatalysator, der omdanner CO2 til ethylen. Kredit:Canadisk lyskilde Tænk, hvis vi kunne tage CO2, den mest berygtede af drivhusgasser, og konverter det til
Fra drivhusgasser til plast:Ny katalysator til genanvendelse af kuldioxid opdagetOverfladen på en nanostruktureret kobberkatalysator, der omdanner CO2 til ethylen. Kredit:Canadisk lyskilde Tænk, hvis vi kunne tage CO2, den mest berygtede af drivhusgasser, og konverter det til -
 Et skridt tættere på at forstå eksplosiv følsomhed med molekyledesignDaniel Preston (til venstre), Virginia Manner (i midten) og Geoff Brown udarbejder en slagvægtstest på et eksplosivt PETN-derivat. Kredit:Los Alamos National Laboratory Sprængstoffer har et iboend
Et skridt tættere på at forstå eksplosiv følsomhed med molekyledesignDaniel Preston (til venstre), Virginia Manner (i midten) og Geoff Brown udarbejder en slagvægtstest på et eksplosivt PETN-derivat. Kredit:Los Alamos National Laboratory Sprængstoffer har et iboend -
 Modificerede biomaterialer samles selv på temperaturangivelserSelvsamlede strukturer dannet af fedtsyremodificerede elastinlignende polypeptider (FAME). Forskere bruger temperatursignaler til at få molekylerne til at samle sig selv. Kredit:Davoud Mozhdehi og Kel
Modificerede biomaterialer samles selv på temperaturangivelserSelvsamlede strukturer dannet af fedtsyremodificerede elastinlignende polypeptider (FAME). Forskere bruger temperatursignaler til at få molekylerne til at samle sig selv. Kredit:Davoud Mozhdehi og Kel -
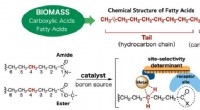 Et nyt værktøj til at skabe kemisk kompleksitet fra fedtsyrerDen nyudviklede katalysator (midterste bund) består af et metal (iridium) atom i kernen og forskellige moduler, der sikrer, at fedtsyreamid eller ester er præcist placeret på en måde, så CH -bindingen
Et nyt værktøj til at skabe kemisk kompleksitet fra fedtsyrerDen nyudviklede katalysator (midterste bund) består af et metal (iridium) atom i kernen og forskellige moduler, der sikrer, at fedtsyreamid eller ester er præcist placeret på en måde, så CH -bindingen
- Hvad fortæller formlen for sammensat magnesiumchlorid mgcl2 dig om, hvor mange ioner der er behov f…
- Hvilken farve observerer du for opløsningen af hydreret kobber (II) chlorid i vand?
- Har Helium Xenon og Neon stabile elektronkonfigurationer?
- Hvorfor skal astronauter træne på den internationale rumstation?
- Hvordan bruger mennesker termisk energi?
- Hvorfor opretstående pingviner afviser deres første æg og lægger et andet


