Hvorfor er chloreddikesyre mere sur end eddikesyre?
* Elektron-tilbagetrækningseffekt: Chloratomet er mere elektronegativt end brint. Dette betyder, at det tiltrækker elektroner mod sig selv og trækker elektrondensitet væk fra carboxylgruppen (-COOH) i chloreddikesyre.
* stabilisering af den konjugatbase: Denne elektron -tilbagetrækning har en afgørende virkning på stabiliteten af den konjugatbase (acetation). I chloreddikesyre spredes den negative ladning på carboxylationen mod chloratomet, hvilket effektivt delokaliserer ladningen. Dette gør konjugatbasen mere stabil.
* surhed: Jo mere stabile konjugatbasen er, jo stærkere er syren. Derfor er chloreddikesyre med sin mere stabile konjugatbase en stærkere syre end eddikesyre.
i enklere termer: Chloratomet hjælper med at "sprede" den negative ladning i den konjugerede base af chloreddikesyre, hvilket gør det mindre sandsynligt, at det genkendes med en proton. Dette gør det mere surt.
Her er en visuel analogi:Forestil dig den negative ladning som en ballon. I eddikesyre er ballonen lille og tæt holdt. I chloreddikesyre fungerer kloratomet som en større ballon, som den negative ladning kan sprede sig i, hvilket gør det mindre sandsynligt, at det kollapser tilbage til sin oprindelige tilstand.
 Varme artikler
Varme artikler
-
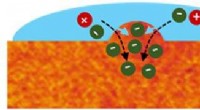 For at forbinde biologi med elektronik, være stiv, alligevel fleksibelEt skematisk billede af P3HT-filmen, viser områder, der er i stand til subtilt at svulme op for at lukke ionmolekyler ind. Kredit:Rajiv Giridharagopal Problemet er en grundlæggende uforenelighed i
For at forbinde biologi med elektronik, være stiv, alligevel fleksibelEt skematisk billede af P3HT-filmen, viser områder, der er i stand til subtilt at svulme op for at lukke ionmolekyler ind. Kredit:Rajiv Giridharagopal Problemet er en grundlæggende uforenelighed i -
 Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan
Ladningsoverførsel inden for overgangsmetalfarvestoffer analyseretEn røntgenimpuls sonderer delokaliseringen af jern-3d-elektroner på tilstødende ligander. Kredit:M. Künsting/HZB Overgangsmetalkomplekser i farvestofbaserede solceller er ansvarlige for at omdan -
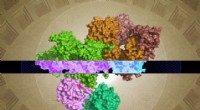 Forskere identificerer molekylær struktur af GATOR1 -proteinkomplekset, der regulerer cellulære væ…Den cryo-EM-genererede GATOR1-struktur kan give indsigt i dens funktion. Kredit:Steven Lee/Whitehead Institute Et team af forskere fra Whitehead Institute og Howard Hughes Medical Institute har af
Forskere identificerer molekylær struktur af GATOR1 -proteinkomplekset, der regulerer cellulære væ…Den cryo-EM-genererede GATOR1-struktur kan give indsigt i dens funktion. Kredit:Steven Lee/Whitehead Institute Et team af forskere fra Whitehead Institute og Howard Hughes Medical Institute har af -
 Hvordan bittesmå enzymer troner øverst i verdensomspændende kulstofgenbrugHvide rådsvampe, Duke Forest, North Carolina Kredit:NA Genanvendelsen af det meste af kulstoffet i naturen afhænger af nedbrydning af to polymerer i træemateriale, især cellulose og lignin. I et
Hvordan bittesmå enzymer troner øverst i verdensomspændende kulstofgenbrugHvide rådsvampe, Duke Forest, North Carolina Kredit:NA Genanvendelsen af det meste af kulstoffet i naturen afhænger af nedbrydning af to polymerer i træemateriale, især cellulose og lignin. I et
- Undersøgelse kan hjælpe med at forklare, hvorfor jern kan forværre malariainfektion
- Krager viser avancerede indlæringsevner
- På hvilke måder understøtter solen livet?
- Stater er begyndt at slå ned på cyberflash, men det er måske ikke nok
- Hvor mange slags væsker er der i verden?
- Fattige menneskers villighed til at stemme påvirkes af lokalsamfundet


