Hvor mange ikke -bindingspar er elektroner i CL4?
Her er hvorfor:
* klor (Cl) er i gruppe 17 (VIIA) i den periodiske tabel, hvilket betyder, at den har 7 valenselektroner.
* For at opnå en stabil oktet har klor brug for endnu en elektron.
* I et hypotetisk CL₄ -molekyle ville hvert kloratom blive bundet til tre andre klor, hvilket danner en tetrahedral struktur. Dette ville efterlade hvert kloratom med kun 3 bindinger og 4 ikke-bindende elektroner (2 ensomme par).
* Imidlertid er dette arrangement meget ustabil . Afvisningen mellem de ensomme par og bindingsparene ville gøre molekylet ekstremt reaktivt.
I stedet for cl₄ tænker du måske på cl₂ (klorgas), der findes som et diatomisk molekyle med et ensomt par på hvert kloratom.
Sidste artikelHvorfor overskydende opløsningsmiddel anvendt i rygtitrering?
Næste artikelSkriv udtrykket og værdien for specifik vandvarme?
 Varme artikler
Varme artikler
-
 En saltopløsning til afsaltning af saltlageKredit:Pixabay/CC0 Public Domain Solcelledrevet saltlagekrystallisering kan afhjælpe miljøpåvirkningerne fra afsaltning af havvand. Behandling af spildlage ved hjælp af en selvrensende krystallis
En saltopløsning til afsaltning af saltlageKredit:Pixabay/CC0 Public Domain Solcelledrevet saltlagekrystallisering kan afhjælpe miljøpåvirkningerne fra afsaltning af havvand. Behandling af spildlage ved hjælp af en selvrensende krystallis -
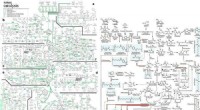 Et omfattende metabolisk kort til produktion af biobaserede kemikalierBiobaseret kemikalieproduktion ad biologiske og kemiske veje. Dette metaboliske kort beskriver repræsentative kemikalier, der kan fremstilles enten ved biologiske og/eller kemiske midler. Røde pile re
Et omfattende metabolisk kort til produktion af biobaserede kemikalierBiobaseret kemikalieproduktion ad biologiske og kemiske veje. Dette metaboliske kort beskriver repræsentative kemikalier, der kan fremstilles enten ved biologiske og/eller kemiske midler. Røde pile re -
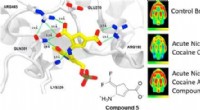 En forbedret medicin mod afhængighedKredit:American Chemical Society Narkotikamisbrug fortsætter med at plage et stort antal mennesker over hele verden, ødelægge og afslutte liv, mens forsøg på at udvikle mere effektive farmaceutisk
En forbedret medicin mod afhængighedKredit:American Chemical Society Narkotikamisbrug fortsætter med at plage et stort antal mennesker over hele verden, ødelægge og afslutte liv, mens forsøg på at udvikle mere effektive farmaceutisk -
 Fremtrædende akademikere efterlyser mere videnskab inden for retsmedicinSalk neuroforsker Thomas Albright studerer syn og hukommelse. Kredit:Salk Instituttet Da retsvidenskaben står over for stigende kontrol, da den spiller en stadig mere fremtrædende rolle i retsplej
Fremtrædende akademikere efterlyser mere videnskab inden for retsmedicinSalk neuroforsker Thomas Albright studerer syn og hukommelse. Kredit:Salk Instituttet Da retsvidenskaben står over for stigende kontrol, da den spiller en stadig mere fremtrædende rolle i retsplej
- Brug af en kraft til at flytte et objekt på tværs af afstand er?
- Ny forskning afdækker vejen til fejlfri tynde film
- Video:Hortensiaer og videnskaben om gør-overs
- Traditionsteori:Hvorfor arkitekt Seiichi Shirai praktiserede kalligrafi
- Er ikke -vaskulære planter bedre egnet til liv på land?
- Langsomt restaurering på brasiliansk museum med brandslukning


