Hvad sker der, når natriumhydroxid tilsættes til kobbersulfatopløsning?
1. Reaktionen:
* Natriumhydroxid (NaOH) er en stærk base, mens kobbersulfat (cuso₄) er et opløseligt salt. Når de reagerer, forekommer en dobbeltfortrængningsreaktion.
* Natriumionerne (Na⁺) fra NaOH kombineres med sulfationerne (SO₄²⁻) fra CUSO₄ til dannelse af natriumsulfat (Na₂so₄), som forbliver opløst i opløsningen.
* Kobberionerne (cu²⁺) fra cuso₄ kombineres med hydroxidionerne (OH⁻) fra NaOH til dannelse af kobber (II) hydroxid (Cu (OH) ₂).
2. Udfældning:
* Kobber (II) Hydroxid (Cu (OH) ₂) er uopløselig i vand, hvilket betyder, at det ikke opløses.
* Som et resultat danner det et solidt bundfald, der fremstår som en blå gelatinøs masse i opløsningen.
Den kemiske ligning:
`` `
Cuso₄ (aq) + 2naoh (aq) → cu (OH) ₂ (s) + na₂so₄ (aq)
`` `
Nøglepunkter:
* Denne reaktion er et klassisk eksempel på en nedbørreaktion .
* Dannelsen af det blå bundfald er en klar indikation af, at reaktionen er sket.
* Opløsningen vil også blive lidt mere grundlæggende (alkalisk) på grund af tilstedeværelsen af overskydende hydroxidioner.
Bemærk: Hvis du fortsætter med at tilsætte natriumhydroxid, vil det blå bundfald til sidst opløses igen, hvilket danner en dyb blå opløsning indeholdende den komplekse ion [Cu (OH) ₄] ²⁻.
 Varme artikler
Varme artikler
-
 Supercomputering af kemiske reaktionerAnimation, der viser den laveste energiovergangstilstand for dannelsen af cyclopentenoner, som findes i et stort antal naturlige produkter, herunder jasminolier, aflatoksiner, og flere prostaglandin
Supercomputering af kemiske reaktionerAnimation, der viser den laveste energiovergangstilstand for dannelsen af cyclopentenoner, som findes i et stort antal naturlige produkter, herunder jasminolier, aflatoksiner, og flere prostaglandin -
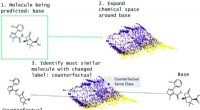 Brug af kontrafakta til at verificere forudsigelser om lægemiddelsikkerhedOversigt over MMACE. Inputtet er et molekyle, der skal forudsiges. Kemisk rum udvides og klynges. Kontrafakta er udvalgt fra klynger for at finde en kortfattet forklaring på forudsigelse af basemoleky
Brug af kontrafakta til at verificere forudsigelser om lægemiddelsikkerhedOversigt over MMACE. Inputtet er et molekyle, der skal forudsiges. Kemisk rum udvides og klynges. Kontrafakta er udvalgt fra klynger for at finde en kortfattet forklaring på forudsigelse af basemoleky -
 Det er smart at sy! Forskere opfinder tråde for at opdage gasser, når de er vævet ind i tøjFøletråde forberedt med bromthymolblåt (overtråd), methylrød (mellemtråd) og MnTPP (bundtråd) udsættes for ammoniak ved 0 ppm (venstre panel), 50 ppm (midterste panel) og 1000 ppm (højre panel). Kredi
Det er smart at sy! Forskere opfinder tråde for at opdage gasser, når de er vævet ind i tøjFøletråde forberedt med bromthymolblåt (overtråd), methylrød (mellemtråd) og MnTPP (bundtråd) udsættes for ammoniak ved 0 ppm (venstre panel), 50 ppm (midterste panel) og 1000 ppm (højre panel). Kredi -
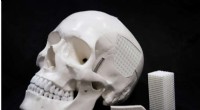 Æggeskalsbaseret kirurgisk materiale til kranieskaderSkalleimplantat. Kredit:NUST MISIS En bioaktiv polymer-keramisk komposit til fiksering af implantater og gendannelse af knogledefekter i kraniet er udviklet af en international gruppe af materiale
Æggeskalsbaseret kirurgisk materiale til kranieskaderSkalleimplantat. Kredit:NUST MISIS En bioaktiv polymer-keramisk komposit til fiksering af implantater og gendannelse af knogledefekter i kraniet er udviklet af en international gruppe af materiale


