Forklar om kondutometrisk af kobbersulfat med natriumhydroxid?
Konduktometrisk titrering af kobbersulfat med natriumhydroxid
Konduktometrisk titrering er en metode, der bruges til at bestemme slutpunktet for en titrering ved at måle den elektriske ledningsevne af opløsningen. I tilfælde af kobbersulfat (cuso₄) og natriumhydroxid (NaOH) involverer reaktionen dannelsen af kobberhydroxidudfældning:
cuso₄ (aq) + 2naoh (aq) → cu (OH) ₂ (s) + na₂so₄ (aq)
Sådan fungerer den ledende titrering:
1. Indledende ledningsevne:
* Den indledende opløsning indeholder kobbersulfat, som er en stærk elektrolyt, hvilket betyder, at den adskiller sig fuldstændigt i ioner (Cu²⁺ og SO₄²⁻) i opløsning. Denne høje koncentration af ioner resulterer i høj elektrisk ledningsevne.
2. Tilsætning af natriumhydroxid:
* Når NaOH tilsættes dråbevis, reagerer det med Cu²⁺ -ioner og danner det uopløselige kobberhydroxid -bundfald (Cu (OH) ₂).
* Fjernelsen af Cu²⁺ -ioner fra opløsningen mindsker konduktiviteten.
* Samtidig er Na⁺ og So₄²⁻ -ioner til stede i opløsningen, hvilket bidrager til konduktiviteten.
3. Ækvivalenspunkt:
* På ækvivalenspunktet har alle Cu²⁺ -ioner reageret med NaOH og dannet bundfaldet.
* Konduktiviteten når et minimum, fordi løsningen primært indeholder na⁺ og so₄²⁻ioner.
4. Post-ækvivalenspunkt:
* Efter ækvivalenspunktet tilføjes overskydende NaOH.
* Dette øger ledningsevnen yderligere på grund af tilstedeværelsen af frie OH⁻ -ioner fra NaOH.
Conductometrisk titreringskurve:
Konduktivitetsændringerne under titreringen kan afbildes mod mængden af NaOH tilføjet. Dette skaber en graf med to lineære segmenter:
* segment 1: En faldende hældning som cu²⁺ ioner reagerer med NaOH.
* segment 2: En stigende hældning efter ækvivalenspunktet på grund af tilsætning af overskydende NaOH.
Krydset mellem disse to segmenter repræsenterer ækvivalenspunktet for titreringen.
Fordele ved ledningsometrisk titrering:
* Velegnet til farvede eller uklare løsninger: I modsætning til visuelle titreringer er det ikke afhængig af farveændring til slutpunktbestemmelse.
* Gælder for svage syrer/baser: Konduktometrisk titrering kan bestemme ækvivalenspunktet selv for svage syrer/baser, som ikke viser en skarp pH -ændring.
* Høj nøjagtighed: Metoden giver mere nøjagtige resultater sammenlignet med visuelle titrationer.
Begrænsninger:
* Kræver specialudstyr (ledningsevne meter).
* Metoden kan påvirkes af temperaturændringer.
Sammenfattende er ledningsometrisk titrering en værdifuld teknik til bestemmelse af ækvivalenspunktet for en reaktion ved at måle ledningsevneændringerne i løsningen. Det er især nyttigt til titreringer, der involverer farvede eller uklare opløsninger, svage syrer/baser og situationer, hvor visuel endepunktbestemmelse er vanskelig.
 Varme artikler
Varme artikler
-
 Undersøgelsen stiller spørgsmålstegn ved blyforgiftningens rolle i Franklin Expeditions dødsfaldI sommeren 1845 under kommando af Sir John Franklin, 128 officerer og besætning ombord på skibene HMS Erebus, over, og HMS Terror kom ind i farvandene i det arktiske Nordamerika med det mål at fuldfør
Undersøgelsen stiller spørgsmålstegn ved blyforgiftningens rolle i Franklin Expeditions dødsfaldI sommeren 1845 under kommando af Sir John Franklin, 128 officerer og besætning ombord på skibene HMS Erebus, over, og HMS Terror kom ind i farvandene i det arktiske Nordamerika med det mål at fuldfør -
 Hvordan metaller arbejder sammen for at svække hårdføre nitrogen-nitrogen-bindingerKredit:CC0 Public Domain nitrogen, et element, der er essentielt for alle levende celler, udgør omkring 78 procent af Jordens atmosfære. Imidlertid, de fleste organismer kan ikke gøre brug af dett
Hvordan metaller arbejder sammen for at svække hårdføre nitrogen-nitrogen-bindingerKredit:CC0 Public Domain nitrogen, et element, der er essentielt for alle levende celler, udgør omkring 78 procent af Jordens atmosfære. Imidlertid, de fleste organismer kan ikke gøre brug af dett -
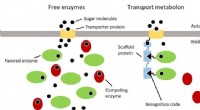 Mere effektiv udnyttelse af råmaterialer ved hjælp af molekylære transportbåndI bagegær, forskellige enzymer konkurrerer om sukkermolekyler, der indføres i cellen af transportproteiner. Således at sukkeret kun omdannes af enzymer, der leverer produkter, der er ønskelige fra e
Mere effektiv udnyttelse af råmaterialer ved hjælp af molekylære transportbåndI bagegær, forskellige enzymer konkurrerer om sukkermolekyler, der indføres i cellen af transportproteiner. Således at sukkeret kun omdannes af enzymer, der leverer produkter, der er ønskelige fra e -
 Forskere afslører robust ethan-fangende porøst organisk bur til effektiv anvendelse af ethylenrens…Kredit:Prof. YUANs gruppe Fjernelse af ethan (C 2 H 6 ) fra dets analoge ethylen (C 2 H 4 ) er af stor betydning i den petrokemiske industri, og er meget udfordrende på grund af deres lign
Forskere afslører robust ethan-fangende porøst organisk bur til effektiv anvendelse af ethylenrens…Kredit:Prof. YUANs gruppe Fjernelse af ethan (C 2 H 6 ) fra dets analoge ethylen (C 2 H 4 ) er af stor betydning i den petrokemiske industri, og er meget udfordrende på grund af deres lign
- Hvorfor blev der ikke nævnt de andre planeter i Bibelen?
- Tekster som netværk:Hvor mange ord er tilstrækkeligt til at identificere en forfatter?
- Hvordan er calciumchlorid smelteis?
- Doping af grafen
- Hvorfor nogle grønne bliver brune i historiske malerier
- Transport af lipidkonjugeret floxuridin med naturligt serumalbumin til levering til kræftceller


