Når ammoniumhydroxidoverskud tilsættes til jernholdigt sulfat?
Første reaktion:
* feso₄ (aq) + 2nh₄oh (aq) → Fe (OH) ₂ (s) + (NH₄) ₂SO₄ (aq)
* Jernsulfat reagerer med ammoniumhydroxid for at danne et lysegrønt bundfald af jernholdigt hydroxid (Fe (OH) ₂).
* Ammoniumsulfat ((NH₄) ₂SO₄) forbliver i opløsning.
Overskydende ammoniumhydroxid:
* M
* Den overskydende ammoniumhydroxid reagerer med det jernholdige hydroxid for at danne en opløselig kompleks ion, hexammineiron (II) ion ([Fe (NH₃) ₆] ²⁺).
* Denne komplekse ion er farveløs.
Oxidation i luft:
* Hexammineiron (II) -ionen er ustabil i luft og oxideres let for at danne et rødbrunt bundfald af jernhydroxid (Fe (OH) ₃).
* 4 [Fe (NH₃) ₆] ²⁺ (aq) + O₂ (g) + 8H₂O (l) → 4Fe (OH) ₃ (s) + 8nh₄⁺ (aq) + 4oh⁻ (aq)
Samlede observationer:
1. indledende grønt bundfald: Dannelsen af den blege grønne jernholdige hydroxid -bundfald er den første synlige reaktion.
2. opløsning af bundfaldet: Med tilsætning af overskydende ammoniumhydroxid opløses bundfaldet på grund af dannelsen af det opløselige hexammineiron (II) -kompleks.
3. rødbrun bundfald: Opløsningen bliver til sidst rødligbrun, når hexammineiron (II) kompleks oxideres i luft og danner jernhydroxid.
Vigtig note: Denne reaktion er et klassisk eksempel på, hvordan overskydende reagens kan føre til dannelse af et andet produkt på grund af kompleks dannelse og efterfølgende oxidation.
 Varme artikler
Varme artikler
-
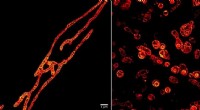 Levende mitokondrier set i hidtil usete detaljer:fotoblegning i STED-mikroskopi overvundetIndre membraner af levende mitokondrier under et STED-mikroskop afbildet ved hjælp af MitoPB Yellow fluorescerende markørmolekyle skabt af forskere ved Institute of Transformative Bio-Molecules (ITbM)
Levende mitokondrier set i hidtil usete detaljer:fotoblegning i STED-mikroskopi overvundetIndre membraner af levende mitokondrier under et STED-mikroskop afbildet ved hjælp af MitoPB Yellow fluorescerende markørmolekyle skabt af forskere ved Institute of Transformative Bio-Molecules (ITbM) -
 Optisk mikroskopstrategi giver observatører mulighed for at kontrollere elektroner, der bevæger si…Kredit:CC0 Public Domain Et hold ledet af DGIST-professor Seo Dae-ha har udviklet en eksperimentel strategi til at kontrollere og observere den kemiske reaktion af en enkelt nanokatalysator ved hjæ
Optisk mikroskopstrategi giver observatører mulighed for at kontrollere elektroner, der bevæger si…Kredit:CC0 Public Domain Et hold ledet af DGIST-professor Seo Dae-ha har udviklet en eksperimentel strategi til at kontrollere og observere den kemiske reaktion af en enkelt nanokatalysator ved hjæ -
 En ny type kemisk binding:Charge-shift-bindingenEt univers af kemiske ligninger. Kredit:Nikolayenko Yekaterina/Shutterstock.com John Morrison Galbraith er lektor i kemi ved Marist College, der studerer kemisk binding, som er den proces, der hol
En ny type kemisk binding:Charge-shift-bindingenEt univers af kemiske ligninger. Kredit:Nikolayenko Yekaterina/Shutterstock.com John Morrison Galbraith er lektor i kemi ved Marist College, der studerer kemisk binding, som er den proces, der hol -
 NIST-software hjælper med analysen af instrumenterede charpy-testsEt skærmbillede fra NICAS, viser en instrumenteret kraft/forskydningskurve for en fuldt duktilt prøve og dens tilsvarende karakteristiske kraftparametre (generelt udbytte, maksimal kraft, slutningen a
NIST-software hjælper med analysen af instrumenterede charpy-testsEt skærmbillede fra NICAS, viser en instrumenteret kraft/forskydningskurve for en fuldt duktilt prøve og dens tilsvarende karakteristiske kraftparametre (generelt udbytte, maksimal kraft, slutningen a
- Hvor meget ville du betale for at fjerne børnearbejde fra din kakao?
- Hvordan Afrika kan øge sit spil med vandforvaltning til landbrug
- Et tip til fremtidig nanoskala -sansning
- Rolling Fourier-ringkorrelationsmetode kortlægger lokal kvalitet i superopløsningsskala
- Den gode, de dårlige og de ensomme:hvordan coronavirus ændrede australsk familieliv
- Hvor stor risiko er du for at få en virus på et fly?


