Hvilken binding dannes ved deling af elektroner mellem atomer, der ikke adskiller sig i deres elektronegativiteter?
Her er hvorfor:
* Elektronegativitet: Elektronegativitet er et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding.
* polær kovalent binding: Når atomer har en signifikant forskel i elektronegativitet, deles elektronerne ulige. Dette skaber en delvis positiv ladning på det ene atom og en delvis negativ ladning på den anden, hvilket resulterer i en polær binding.
* ikke -polær kovalent binding: Når atomer har lignende eller lige elektroniske, elektronerne deles lige. Der er ingen adskillelse af ladning, og bindingen betragtes som ikke -polær.
Eksempler på ikke -polære kovalente obligationer:
* h-h (brintgas)
* cl-cl (klorgas)
* o =o (iltgas)
 Varme artikler
Varme artikler
-
 Ny katalysator overstråler platin til fremstilling af brintKredit:CC0 Public Domain Brint, det mest udbredte element i universet, giver et stærkt slag. Og fordi det ikke indeholder kulstof, det producerer kun vand, når det bruges som brændstof. Men på jor
Ny katalysator overstråler platin til fremstilling af brintKredit:CC0 Public Domain Brint, det mest udbredte element i universet, giver et stærkt slag. Og fordi det ikke indeholder kulstof, det producerer kun vand, når det bruges som brændstof. Men på jor -
 Springende og holdbare gummibelægninger kan redde tusinder af liv, siger forskereKredit:Astrid Gast, Shutterstock Et team af forskere støttet af et EU -initiativ tester belægninger lavet af genbrugsdæk for at forhindre skader som følge af ulykker og fald. Fald og faldrelatere
Springende og holdbare gummibelægninger kan redde tusinder af liv, siger forskereKredit:Astrid Gast, Shutterstock Et team af forskere støttet af et EU -initiativ tester belægninger lavet af genbrugsdæk for at forhindre skader som følge af ulykker og fald. Fald og faldrelatere -
 Nye fotokatalysatorer kan udføre solcelledrevet omdannelse af kuldioxid til brændstofVedtagelse af den fotokatalytiske omdannelse af CO2 til brændstof i højemissionsanlæg ville være yderst gavnlig for både miljøet og økonomien. Kredit:Shutterstock Forskere ved Daegu Gyeongbuk Inst
Nye fotokatalysatorer kan udføre solcelledrevet omdannelse af kuldioxid til brændstofVedtagelse af den fotokatalytiske omdannelse af CO2 til brændstof i højemissionsanlæg ville være yderst gavnlig for både miljøet og økonomien. Kredit:Shutterstock Forskere ved Daegu Gyeongbuk Inst -
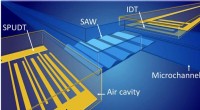 NIST-opdagelse kan øge nøjagtigheden ved måling af blodgennemstrømning til kræftdiagnose, andre…Akustiske overfladebølger (SAW) bevæger sig gennem en mikrovæske begrænset til et hulrum eller en mikrokanal og analyseres derefter af modtageren. Både den akustiske bølgesender (SPUDT) og modtageren
NIST-opdagelse kan øge nøjagtigheden ved måling af blodgennemstrømning til kræftdiagnose, andre…Akustiske overfladebølger (SAW) bevæger sig gennem en mikrovæske begrænset til et hulrum eller en mikrokanal og analyseres derefter af modtageren. Både den akustiske bølgesender (SPUDT) og modtageren
- Hvad kaldes tab af overskydende vand og salt fra kroppen?
- Ændrer konstellationer afhængigt af det land, du ser dem fra?
- Energiindholdet i et stykke mad bestemmes af?
- Hvordan adskiller skaden forårsaget af udbrud af Mt Pinatubo sig fra udbrud St Helen?
- Sådan forhindrer du arbejdere i at blive udnyttet i koncertens økonomi
- Videnskab-hvad er en anden betegnelse for stater?


