Hvorfor bruger du smeltet NaCI i elektrolyse i stedet for en vandig opløsning NaCl?
smeltet NaCl -elektrolyse:
* Produkt: Det primære produkt er natriummetal (NA) , som er et meget reaktivt element. Dette er ikke muligt med en vandig opløsning, fordi vand ville reagere med natrium.
* Betingelser: Kræver høje temperaturer (over 801 ° C) for at smelte NaCl, hvilket er energikrævende.
* bivirkninger: Ingen, da der ikke er andre ioner til stede bortset fra Na+ og Cl-.
* applikationer: Primært brugt i den industrielle produktion af natriummetal.
vandig NaCl -elektrolyse:
* Produkter: Produkterne er brintgas (H2) Ved katoden og klorgas (CL2) Ved anoden.
* Betingelser: Kan udføres ved stuetemperatur og tryk, meget mere energieffektivt end at bruge smeltet salt.
* bivirkninger: Vand er også elektrolyseret, hvilket fører til dannelse af brint og ilt. Dette kan være et ønsket eller uønsket produkt afhængigt af applikationen.
* applikationer: Brugt til produktion af klorgas og natriumhydroxid (NaOH) såvel som i forskellige elektrokemiske anvendelser.
Kortfattet:
* smeltet NaCl: Bruges, når det primære mål er at producere natriummetal. Det er en specialiseret proces med høje energibehov.
* vandig NaCl: Bruges, når målet er at fremstille klorgas, brintgas eller natriumhydroxid. Dette er en mere almindelig og alsidig proces.
Valg af den rigtige metode:
Valget af, hvilken metode der skal bruges, afhænger af de ønskede produkter. Hvis du vil have natriummetal, skal du bruge smeltet NaCl. Hvis du vil have klor eller brint, er en vandig opløsning mere effektiv.
Sidste artikelEr natriumchlorid en termisk ledningsevne?
Næste artikelEr salt og sukker en blanding eller opløsning?
 Varme artikler
Varme artikler
-
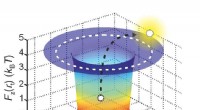 Den første præcise måling af et enkelt molekyls effektive ladningForskere kan bestemme den effektive elektriske ladning af et molekyle ved at fange det i en potentiel brønd ved at måle, hvor længe det bliver inde. Kredit:Madhavi Krishnan / University of Zurich
Den første præcise måling af et enkelt molekyls effektive ladningForskere kan bestemme den effektive elektriske ladning af et molekyle ved at fange det i en potentiel brønd ved at måle, hvor længe det bliver inde. Kredit:Madhavi Krishnan / University of Zurich -
 Under pres, brint giver en afspejling af kæmpe planetinteriørJoviansk skylandskab, med tilladelse fra NASAs Juno -rumfartøj. Kredit:NASA/JPL-Caltech/SwRI/MSSS/Gerald Eichstädt/Seán Dora Lab-baseret efterligning tillod et internationalt team af fysikere, her
Under pres, brint giver en afspejling af kæmpe planetinteriørJoviansk skylandskab, med tilladelse fra NASAs Juno -rumfartøj. Kredit:NASA/JPL-Caltech/SwRI/MSSS/Gerald Eichstädt/Seán Dora Lab-baseret efterligning tillod et internationalt team af fysikere, her -
 Hvad hvis flyvemaskiner kunne reparere deres egen skade?Kredit:Pixabay. Flyvemaskiner er himmelstrøg; et kommercielt passagerfly er over 6, 000 gange så tung som en stor canadisk gås. Ved 500 mph, imidlertid, disse besætninger er ikke uigennemtrængelig
Hvad hvis flyvemaskiner kunne reparere deres egen skade?Kredit:Pixabay. Flyvemaskiner er himmelstrøg; et kommercielt passagerfly er over 6, 000 gange så tung som en stor canadisk gås. Ved 500 mph, imidlertid, disse besætninger er ikke uigennemtrængelig -
 Team udvikler nye måder at skabe og levere medicin til en bred vifte af immunmedicinske neuropatierKredit:Liverpool School of Tropical Medicine Forskere ved LSTM ser på nye måder at skabe og levere medicin til en bred vifte af immunmedicinerede neuropatier, ved at udvikle nye syntetiske version
Team udvikler nye måder at skabe og levere medicin til en bred vifte af immunmedicinske neuropatierKredit:Liverpool School of Tropical Medicine Forskere ved LSTM ser på nye måder at skabe og levere medicin til en bred vifte af immunmedicinerede neuropatier, ved at udvikle nye syntetiske version
- Sådan konverteres tiendedele til tommer
- Hvilken energitransformation er ansvarlig for den fyrige reentry af rumfærgen i atmosfæren?
- Bestemmelse af koncentrationen af koncentreret saltsyre?
- California Desert Animals & Desert Plants
- Watchdog:FBI kunne have prøvet hårdere på at hacke iPhone
- En tabel udøver en 4,0 kg Newton -styrke på bogen, der ligger ved hvile, den udøves af IS?


