Hvorfor er de ædle gasser relativt ureaktive?
* Fuld valensskaller: Ædle gasser har en komplet yderste elektronskal (også kendt som valensskallen). Dette betyder, at de har det maksimale antal elektroner, som deres energiniveau kan have.
* stabil octet: De fleste ædle gasser (undtagen helium) har otte elektroner i deres valensskal, hvilket opnår en stabil "octet" -konfiguration. Denne ordning gør dem ekstremt stabile og modstandsdygtige over for at vinde eller miste elektroner.
* Høj ioniseringsenergier: Fjernelse af et elektron fra et ædelgasatom kræver en betydelig mængde energi, hvilket gør det meget usandsynligt at forekomme. Dette skyldes, at den stærke tiltrækning mellem kernen og elektronerne gør det vanskeligt at fjerne dem.
* Lav elektronaffinitet: Noble gasser har meget lav elektronaffinitet, hvilket betyder, at de ikke let accepterer ekstra elektroner. Dette skyldes igen stabiliteten af deres elektronkonfigurationer.
I sammendraget fører den fulde valensskal og stabile elektronkonfigurationer af ædelgasser til deres lave reaktivitet. De er tilfredse i deres tilstand og har ringe tendens til at deltage i kemiske reaktioner.
Sidste artikelHvad er to ikke -nongaseous partikler i luft?
Næste artikelHvad er det kemiske symbol for et inert element?
 Varme artikler
Varme artikler
-
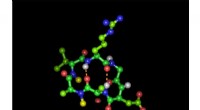 Den hellige gral af peptidkemi:Gør peptidaktive midler tilgængelige oraltCyklisk hexapeptid i sin bioaktive form med den integrinbindende tripeptidsekvens arginin-glycin-asparaginsyre:Grønne kugler repræsenterer carbonatomer, røde iltatomer, blå nitrogenatomer og hvide bri
Den hellige gral af peptidkemi:Gør peptidaktive midler tilgængelige oraltCyklisk hexapeptid i sin bioaktive form med den integrinbindende tripeptidsekvens arginin-glycin-asparaginsyre:Grønne kugler repræsenterer carbonatomer, røde iltatomer, blå nitrogenatomer og hvide bri -
 Nysyntetiseret AM-III kulstof er det hårdeste og stærkeste amorfe materiale til datoHårdhed af AM carbon materialer, sammenlignet med andre kendte amorfe materialer, og ridser på diamant (001) flade indtrukket af AM-III. Kredit: National Science Review (2021). DOI:10.1093/nsr/nwab14
Nysyntetiseret AM-III kulstof er det hårdeste og stærkeste amorfe materiale til datoHårdhed af AM carbon materialer, sammenlignet med andre kendte amorfe materialer, og ridser på diamant (001) flade indtrukket af AM-III. Kredit: National Science Review (2021). DOI:10.1093/nsr/nwab14 -
 Forskere opdager en ny vej til dannelse af komplekse krystallerForskere brugte avancerede mikroskopiteknikker til at se mesokrystaller dannes i realtid. Kredit:Sammensat billede af Mike Perkins | Pacific Northwest National Laboratory Når materialer når ekstre
Forskere opdager en ny vej til dannelse af komplekse krystallerForskere brugte avancerede mikroskopiteknikker til at se mesokrystaller dannes i realtid. Kredit:Sammensat billede af Mike Perkins | Pacific Northwest National Laboratory Når materialer når ekstre -
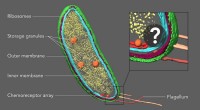 Ny teknik udpeger placeringer af individuelle molekyler i deres cellulære kvartererForskere fra Stanford University troede, at et tilsyneladende tomt område i den ene ende af Caulobacter-bakterien kunne indeholde to proteiner involveret i celledeling. Ved at mærke proteinerne med fl
Ny teknik udpeger placeringer af individuelle molekyler i deres cellulære kvartererForskere fra Stanford University troede, at et tilsyneladende tomt område i den ene ende af Caulobacter-bakterien kunne indeholde to proteiner involveret i celledeling. Ved at mærke proteinerne med fl


