Hvordan kan væsker blive gasser og væsker?
væsker til gasser (fordampning)
* Fordampning: Dette er en langsom proces, hvor flydende molekyler får nok energi fra deres omgivelser til at flygte ind i gasfasen. Det forekommer ved overfladen af væsken og påvirkes af temperatur, overfladeareal og fugtighed.
* kogning: Dette er en hurtigere proces, hvor væsken når en specifik temperatur kaldet dens kogepunkt. På dette tidspunkt er væskens damptryk for det omgivende atmosfæriske tryk, og dampbobler dannes i væsken, hvilket får den til hurtigt at ændre sig til gas.
væsker til faste stoffer (frysning)
* Frysning: Når en væske afkøles under dens frysepunkt, mister dens molekyler energi og bremser. De mister deres evne til at bevæge sig frit, og molekylerne arrangerer sig selv i en mere ordnet, fast struktur og danner et fast stof.
her er en simpel analogi:
Forestil dig en gruppe mennesker, der danser i et overfyldt rum. De bevæger sig frit (som flydende molekyler).
* Fordampning: Nogle mennesker keder sig måske og forlader rummet (som molekyler, der slipper ud i gasfasen).
* kogning: Hvis rummet bliver for varmt (stigende temperatur), vil alle begynde at hoppe rundt vildt (øget molekylær bevægelse) og måske endda skubbe hinanden ud af døren (kogning).
* Frysning: Hvis rummet bliver meget koldt (lavere temperatur), vil alle bremse og til sidst stoppe med at danse og danne en mere organiseret, stationær gruppe (frysning).
Nøglepunkter:
* temperatur er afgørende: Temperatur påvirker energien fra molekyler og påvirker deres stofstilstand.
* tryk spiller en rolle: Tryk kan også påvirke kogepunktet for en væske. Højere tryk betyder et højere kogepunkt.
* statens ændring er reversibel: En solid kan smelte tilbage i en væske, og en gas kan kondensere tilbage til en væske.
Sidste artikelHvad er alle væsker?
Næste artikelHar væsker en egen form?
 Varme artikler
Varme artikler
-
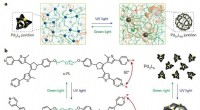 Lysstyrede polymerer kan skifte mellem robuste og blødeDesign af polyMOCer med fotoskiftbar topologi. Kredit:(c) Natur (2018). DOI:10.1038/s41586-018-0339-0 MIT -forskere har designet et polymermateriale, der kan ændre dets struktur som reaktion på
Lysstyrede polymerer kan skifte mellem robuste og blødeDesign af polyMOCer med fotoskiftbar topologi. Kredit:(c) Natur (2018). DOI:10.1038/s41586-018-0339-0 MIT -forskere har designet et polymermateriale, der kan ændre dets struktur som reaktion på -
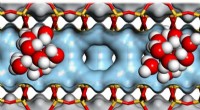 Katalyserer omdannelsen af biomasse til biobrændstofKlynger af vandmolekyler i zeoliternes hulrum hjælper med at katalysere omdannelsen af biomasse til biobrændstof. Kredit:Andreas Jentys / TUM Zeolitter er ekstremt porøse materialer:Ti gram kan
Katalyserer omdannelsen af biomasse til biobrændstofKlynger af vandmolekyler i zeoliternes hulrum hjælper med at katalysere omdannelsen af biomasse til biobrændstof. Kredit:Andreas Jentys / TUM Zeolitter er ekstremt porøse materialer:Ti gram kan -
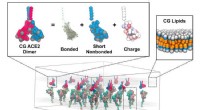 Supercomputersimuleringer afslører detaljerne om coronavirusfusionMekanismen, hvorved coronavirus smelter sammen med værtsceller, er blevet foreslået gennem simuleringer af forskere fra University of Chicago, der bruger Frontera-supercomputeren ved TACC. Repræsentat
Supercomputersimuleringer afslører detaljerne om coronavirusfusionMekanismen, hvorved coronavirus smelter sammen med værtsceller, er blevet foreslået gennem simuleringer af forskere fra University of Chicago, der bruger Frontera-supercomputeren ved TACC. Repræsentat -
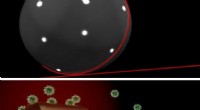 At sætte fokus på livets maskineriEn sensor på en sensor:Laserlys (rødt) skinner (øverst) ind i en mikroperle af glas, som en guld nanorod er fastgjort til. Laserlyset løber rundt om indersiden af mikroperlen og er koncentreret om g
At sætte fokus på livets maskineriEn sensor på en sensor:Laserlys (rødt) skinner (øverst) ind i en mikroperle af glas, som en guld nanorod er fastgjort til. Laserlyset løber rundt om indersiden af mikroperlen og er koncentreret om g
- Er genet vigtigt for organisme eller ej?
- Katastrofe amerikanske orkaner siden 2000. Kunne Harvey toppe dem?
- Cloud computing får ny betydning for forskere
- Kan en 500 mA -transformer bruges til at betjene kredsløb, der kræver 1AMP12W?
- Skolenedlæggelser øger den digitale kløft for eleverne
- Antarktisfaktoren:Modelusikkerheder afslører kommende havniveaurisiko


