Hvilken er større en arsenion eller en bromion?
* ioniske størrelse tendenser: Ionstørrelse øges generelt, når du bevæger dig ned ad en gruppe (kolonne) på den periodiske tabel og falder, når du bevæger dig over en periode (række).
* arsen (AS) og brom (BR): Arsen er i gruppe 15, og brom er i gruppe 17. Dette betyder, at arsen er længere nede på det periodiske tabel end brom.
Derfor er en arsenion (As³⁻) større end en bromion (br⁻).
Forklaring:
* Bevæger sig ned ad en gruppe øges antallet af elektronskaller, hvilket fører til større atom- og ionisk radier.
* Bevægelse af en periode øges antallet af protoner i kernen, tiltrækker elektronerne stærkere og resulterer i en mindre atom- og ionisk radier.
Sidste artikelHvad er metallerne på periodisk tabel?
Næste artikelHvad er antallet og typen af atom i 3 H2O?
 Varme artikler
Varme artikler
-
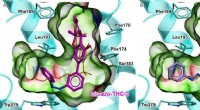 Berusende lysfølsommeTo lysfølsomme THC -derivater, og hvordan de er indlejret i cannabinoidreceptoren 1. Kredit:fra Westphal MV et al. J. Am. Chemical Soc., 2017, 139 (50), s. 18206-18212. ETH -kemikere har syntetise
Berusende lysfølsommeTo lysfølsomme THC -derivater, og hvordan de er indlejret i cannabinoidreceptoren 1. Kredit:fra Westphal MV et al. J. Am. Chemical Soc., 2017, 139 (50), s. 18206-18212. ETH -kemikere har syntetise -
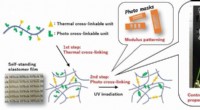 Udvikling af film med justerbar forlængelse og brud til forskellige formålDobbelt-termisk og foto-tværbinding af polymerkæder til syntese af alsidig elastomer. Forskere fra Japan formåede at udvikle en elastomerfilm med justerbar elasticitet ved hjælp af en to-trins termisk
Udvikling af film med justerbar forlængelse og brud til forskellige formålDobbelt-termisk og foto-tværbinding af polymerkæder til syntese af alsidig elastomer. Forskere fra Japan formåede at udvikle en elastomerfilm med justerbar elasticitet ved hjælp af en to-trins termisk -
 Ingeniører identificerer forbedrede membraner til at opfange CO2 på kulfyrede kraftværkerAfbildning af en metalorganisk ramme (HKUST-1) indlejret i en polymermatrix, der skal bruges som membran til effektiv gasseparation. Kredit:Kutay Sezginel/Hypothetical Materials Lab En beregningsm
Ingeniører identificerer forbedrede membraner til at opfange CO2 på kulfyrede kraftværkerAfbildning af en metalorganisk ramme (HKUST-1) indlejret i en polymermatrix, der skal bruges som membran til effektiv gasseparation. Kredit:Kutay Sezginel/Hypothetical Materials Lab En beregningsm -
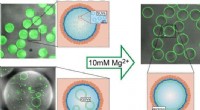 Cellelignende lipidvesikler, som kan udfyldes med naturlige celleproteinerLipidvesikler (til venstre:LUVer eller GUVer; grøn) blev indkapslet i copolymerstabiliserede dråber. Vesiklerne kan transformeres til et lipid-dobbeltlag ved den copolymerstabiliserede dråbe indre græ
Cellelignende lipidvesikler, som kan udfyldes med naturlige celleproteinerLipidvesikler (til venstre:LUVer eller GUVer; grøn) blev indkapslet i copolymerstabiliserede dråber. Vesiklerne kan transformeres til et lipid-dobbeltlag ved den copolymerstabiliserede dråbe indre græ
- Hvordan småkagen smuldrer:Røntgenteknologi plejede at afsløre hemmeligheder bag perfekt kiks
- NTU-spin-off opnår gennembrud med innovative multifunktionsmembraner
- Spørgsmål og svar:Kommende globale strejker, stigende ungdomsprotester, og bekymringen over sundhe…
- Sandheden om misinformation
- Undersøgelse finder potentielt farlige niveauer af arsen i det californiske fængsels drikkevand
- Video:Hvordan dannes snefnug?


