Atomcarbon indeholder hvor mange uparrede elektroner i henhold til regel?
1. Elektronkonfiguration:
* Carbon har et atomnummer på 6, hvilket betyder, at det har 6 elektroner.
* Elektronkonfigurationen af kulstof er 1S² 2S² 2p².
2. Hunds regel:
* Hunds regel siger, at elektroner individuelt vil besætte hver orbital inden for et underskal, før de fordobles i en orbital.
3. Anvendelse af Hunds regel:
* Subshellet 2p har tre orbitaler (2px, 2py, 2pz).
* Carbon har to elektroner i underskalet 2p.
* Ifølge Hunds regel vil disse to elektroner besætte separate 2p orbitaler, hvilket efterlader en 2p orbital tom.
4. Uparrede elektroner:
* Da en 2p orbital forbliver tom, har atomcarbon to uparrede elektroner .
Derfor har atomcarbon to uparrede elektroner.
Sidste artikelHvorfor er silica en gas?
Næste artikelHvad kaldes det, når brint kombineres med brint?
 Varme artikler
Varme artikler
-
 Kemikere opdager en plausibel opskrift på tidligt liv på JordenKredit:CC0 Public Domain Kemikere ved The Scripps Research Institute (TSRI) har udviklet en fascinerende ny teori for, hvordan livet på Jorden kan være begyndt. Deres eksperimenter, beskrevet i d
Kemikere opdager en plausibel opskrift på tidligt liv på JordenKredit:CC0 Public Domain Kemikere ved The Scripps Research Institute (TSRI) har udviklet en fascinerende ny teori for, hvordan livet på Jorden kan være begyndt. Deres eksperimenter, beskrevet i d -
 Fotokrome vismutkomplekser viser et stort løfte for optiske hukommelseselementerKredit:Pixabay/CC0 Public Domain Russiske kemikere har fået et nyt fotokromt kompleks bestående af vismut (III) og viologenkationer og brugt den nye forbindelse til at skabe optiske hukommelsesele
Fotokrome vismutkomplekser viser et stort løfte for optiske hukommelseselementerKredit:Pixabay/CC0 Public Domain Russiske kemikere har fået et nyt fotokromt kompleks bestående af vismut (III) og viologenkationer og brugt den nye forbindelse til at skabe optiske hukommelsesele -
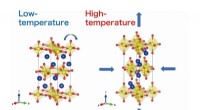 Undersøgelse undersøger bemærkelsesværdig negativ termisk ekspansion set i lagdelte ruthenaterDe strukturelle forvrængninger i Ca 2 RuO 4 er ansvarlige for dens anisotrope termiske ekspansion. Kredit:Masaki Azuma fra Tokyo Institute of Technology En tidligere ubemærket monoklinisk forv
Undersøgelse undersøger bemærkelsesværdig negativ termisk ekspansion set i lagdelte ruthenaterDe strukturelle forvrængninger i Ca 2 RuO 4 er ansvarlige for dens anisotrope termiske ekspansion. Kredit:Masaki Azuma fra Tokyo Institute of Technology En tidligere ubemærket monoklinisk forv -
 Datadeling er fremtiden for materialeforskningKredit: Avanceret Videnskab Brug af data til at designe og udvikle helt nye materialer er et hastigt voksende videnskabsområde. En gruppe forskere ved Aalto-universitetet har netop offentliggjort
Datadeling er fremtiden for materialeforskningKredit: Avanceret Videnskab Brug af data til at designe og udvikle helt nye materialer er et hastigt voksende videnskabsområde. En gruppe forskere ved Aalto-universitetet har netop offentliggjort
- Hvad er generering af alle hybrider produceret ved at krydse to rene organismer?
- Hvad er årsagen til månens faser?
- Hvordan adskiller videnskabsmand en mineraler fra hinanden?
- En ny type brand, brændstoffremtiden?
- 13 døde, da oversvømmelser rammer det sydvestlige Frankrig
- Hvad er massen af et atom koncentreret om?


